印度株
」 變異株
防Delta突破性感染 台大搶先研發薪冠噴鼻疫苗
全球新冠肺炎疫苗兩劑覆蓋率邁向五成,但疫情仍持續延燒,問題癥結點在於現行疫苗皆是對付武漢株,而非目前主流印度株Delta,台大醫院團隊研發專利疫苗佐劑,設計出Delta變異株的關鍵抗原,並投入中和抗體與噴鼻疫苗研發,有助於避免突破性感染,即使未來再有變異株,也能立刻修改部分結構來因應。最快能於一個月內開發出針對Delta株的中和抗體試劑原型。台大醫院研發鼻噴式疫苗,在小鼠實驗發現對降低上呼吸道的病毒量降效果十分顯著。(圖/黃立民提供)台大醫院今天舉辦第2代COVID-19(2019冠狀病毒疾病)疫苗開發新佐劑、新抗原、新投予途徑、中和抗體快速檢測記者會。台大研究團包含台大兒童醫院院長黃立民、台大醫學檢驗部張淑媛、台大獸醫系教授陳慧文,半年前開始投入研發噴鼻式疫苗,並設計出以Delta變異株的棘蛋白受體結合域(RBD)三聚體做為抗原,可以用來開發對抗Delta變異株的疫苗與中和抗體試劑。研究計畫主持人黃立民指出,全球COVID-19疫苗已接種逾70億劑,但疫情仍未見盡頭,主因在於,目前獲核准的疫苗都採肌肉注射、且針對原始的武漢病毒株設計,而非主流的Delta,但病毒不斷變異,所有測量東西都失真,必須重新洗牌。「最好的攻擊就是病毒一進來就開始主動攻擊,而不是等到病毒已經進到氣管一兩周後才開始攻擊」,黃立民解釋,自然感染的模式,就是病毒從鼻腔開始進到肺部,而傳統肌肉注射疫苗只能在肺部產生抗體,雖能降低肺炎重症風險,但上呼吸道仍存在病毒,還是會感染且傳染他人。然而,噴鼻疫苗則模仿自然感染,在鼻腔就能產生獨有的IgA抗體,也能在下呼吸道生成IgG抗體,等於病毒一進到鼻腔就會開始被攻擊,能有效降低上呼吸道病毒量與病毒傳播,並減少Delta變異株的突破性感染。黃立民表示,目前世界都將希望放在噴鼻式疫苗上,目前國際上有7家廠商正在研發鼻噴劑疫苗。台大團隊研發的噴鼻疫苗,運用自行研發的專利黏膜佐劑技術,初步透過小鼠實驗顯示,可有效提升小鼠血清中棘蛋白特異性抗體及中和抗體,優於目前的肌肉注射疫苗,有潛力對付任何變異株病毒。至於噴鼻疫苗的使用對象,可從小孩到49歲成人,副作用是引起局部免疫反應,黃立民指出,理論上副作用會比肌肉注射疫苗還小,過去流感噴鼻疫苗曾發生顏面神經麻痺的副作用,但已知是佐劑是太強導致,研發上可完全避免。此外,台大團隊設計的Delta病毒株RBD三聚體,可用於中和抗體試劑開發,黃立民指出,目前如要測出中和抗體,都必須到P3實驗室才能進行,但現在團隊開發出可測量Delta病毒株中和抗體的ELISA套組,以WHO的血清範本做測試可發現,測武漢株,中和抗體較高,但如碰到Delta株,抗體就會下降,可顯示對抗武漢株的抗體對Delta株無效,能正確反應第三級實驗室的中和抗體,不需進P3實驗室就能檢驗,預計1至2個月後可開發出試劑原型。
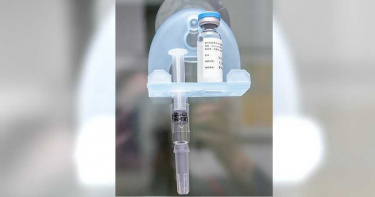
高端疫苗EUA會議記錄曝光 「對Delta病毒效果差」10專家認應做三期
高端疫苗7/19通過緊急使用授權審查EUA,過了將近半個月,食藥署今天終於公布高端疫苗緊急授權的疫苗專家審查會議會議紀錄,本次的會議紀錄並未將參與審查的專家具名,而是以匿名的方式呈現專家意見。出席會議的專家總計21人,主席不參與投票,通過3人、有條件通過15 人、補件再議1人、不通過1人。其中至少有8位專家認為不能只看中和抗體,希望高端補足有關T細胞相關的反應數據;另有專家明確表示,除了中和抗體外,高端應取得有國際認可的免疫標劑biomarker(s)再申請EUA比較適當。這份報告也指出,高端疫苗對武漢株、D614G與巴西(Gamma)病毒株的結果較佳,對南非株(Beta)及印度株(Delta)較差,專家中至少有4人提出應增加對印度株(Delta)保護力驗證。另外,至少有10位專家建議,高端疫苗需補做三期臨床試驗的相關資料。也有專家建議,高端疫苗應蒐集孕婦、衰弱族群的安全性須後續進一步蒐集資料,針對仿單核定問題,適應症請加註年齡,不良反應的部分請 CDE (財團法人醫藥品查驗中心)針對婦女懷孕期及其他不良反應部分再做確認。
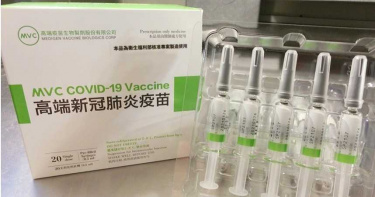
真要打了 ?食藥署同時發佈高端EUA會議內容 宣布首批高端疫苗將完成檢驗
高端疫苗爭議風雲再起!繼高端疫苗日前獲得食藥署給予緊急授權EUA後,食藥署今天公佈去識別化的高端疫苗EUA會議過程紀錄,並宣布,首4批高端疫苗已經完成檢驗並核發封緘證明書,共26萬5528劑高端疫苗正在進行封緘作業,預計今晚就會放行,至於何時提供民眾接種,將由指揮中心拍板決定。值得注意的是,根據高端疫苗EUA會議記錄,多位專家在會中質疑高端疫苗對於變種病毒的保護力,建議應該繼續做第三期實驗以完全確定對變種病毒保護力。另一爭議是,食藥署7月19日才同意給高端疫苗EUA,食藥署強調每批高端疫苗都需要約30到35日的檢驗時間,但食藥署今天卻宣布第一批高端疫苗傍晚就會放行,若回推30日,顯示高端疫苗早在7月19日食藥署通過高端疫苗緊急授權前,高端似乎是先將疫苗送入食藥署檢驗。食藥署今天同時宣佈26萬5528劑高端疫苗正在進行封緘作業,預計今晚就會放行,並同時公佈高端EUA的去識別化會議記錄,引發前北市長郝龍斌強烈不滿,到法院申請緊急停止衛福部對高端的EUA授權。(圖/報系資料照、臉書)雖然食藥署與陳時中都宣稱,廠商原本就能先將藥品疫苗送到食藥署檢驗,如果EUA沒過就會銷毀,但食藥署是否給了高端特殊待遇、其它藥廠生產的疫苗或藥品是否都都能得到像高端「先送檢」的「綠燈」待遇,再次引發議論。針對首批高端疫苗將完成檢驗,前衛生署長楊志良、前台北市長郝龍斌今天宣布,要共同向台北高等行政法院遞狀,聲請法院停止衛福部對高端疫苗的緊急使用授權(EUA),以保障國民健康。食藥署今天宣布放行的四批高端疫苗批號,共26.5萬劑,批號依序為SP2106、SP2107、SP2111及SP2112,針對外界質疑「批號不連續」,中央流行疫情指揮中心指揮官陳時中今天在記者會中證實,每種疫苗產品送到衛福部驗時批號都是連貫的,中間有跳號狀況恐是因為技術性資料不齊全,因此,將等廠商完成補件後,再進行檢驗,暗示第一批完成檢驗的高端疫苗要接種,還得再等等。食藥署今天同時宣佈26萬5528劑高端疫苗正在進行封緘作業,預計今晚就會放行,並同時公佈高端EUA的去識別化會議記錄,引發前北市長郝龍斌強烈不滿,到法院申請緊急停止衛福部對高端的EUA授權。(圖/報系資料照、臉書)陳時中還說,外界對於高端疫苗率先於通過EUA(緊急使用授權)前就已進行量產並送審檢驗,有所質疑。他也解釋,如果等到通過EUA才進行量產,恐怕國產疫苗要等很久才能量產,由於量產並不一定會通過EUA,再加上未通過EUA提前生產疫苗必須銷毀,食藥署的處理沒有問題。食藥署今天宣布,已在7月30日傍晚完成高端疫苗生產的首4批COVID-19疫苗、共計26萬5528劑的審查與檢驗並核發封緘證明書,目前正在倉儲進行檢驗封緘作業,預計傍晚可以放行。不過,這批疫苗何時開打,要由衛福部宣布。食藥署說明,高端疫苗檢驗封緘需耗時近1個月,因疫苗是蛋白質疫苗,和先前國內使用的腺病毒載體、mRNA疫苗檢驗項目不同,除了效價試驗須用動物試驗進行,必須進行21天,確認疫苗保護力,還要同時檢查外觀、鑑別、pH值、鋁含量、CpG含量、總蛋白量、抗原含量、細菌內毒素、無菌、效價及異常毒性等。據食藥署規定,封緘完畢的疫苗都須有EUA才能放行,至於為何高端疫苗還沒通過EUA就能先行送驗?食藥署未說明,由陳時中出面解釋。除此之外,食藥署今天也公佈高端EUA會議的去識別化記錄,根據這份記錄顯示,此次會議出席專家共21人,除主席不參與投票外,通過三人、有條件通過15人、補件再議1人、不通過1人。食藥署今天同時宣佈26萬5528劑高端疫苗正在進行封緘作業,預計今晚就會放行,並同時公佈高端EUA的去識別化會議記錄,引發前北市長郝龍斌強烈不滿,到法院申請緊急停止衛福部對高端的EUA授權。(圖/報系資料照、臉書)雖然最後決議是有條件通過專案製造,但與會專家中,多數專家認為高端疫苗,還必須繼續進行第三期或第三劑追加試驗,並須確認中和抗體以外的免疫效果,如T細胞反應等。此外,會中有專家明確表示,除了中和抗體外,應取得有國際認可的生物標記(biomarker)再申請EUA比較妥當。另有四名專家表示,高端疫苗對於變異株的保護有待確認,因高端疫苗對武漢株、巴西株結果較佳,但對Beta變種病毒(南非株)和Delta變種病毒(印度株)較差,建議應增加相關保護力驗證。針對高端疫苗爭議再起,前台北市長郝龍斌及前衛生署署長楊志良今天召開記者會,宣布將向台北高等行政法院遞狀,聲請法院停止衛福部對高端疫苗的緊急使用授權(EUA),確保國民健康。楊志良強調,Delta變種病毒來勢洶洶,疫苗覆蓋率須到達8成,才有群體免疫力,若高端疫苗欠缺充足防護力,導致11%(約250萬人口)接種高端疫苗的國人成為防疫破口,衛福部扛得起這責任嗎?郝龍斌則表示,政府以「免疫橋接」為藉口,同意高端不用進行第3期試驗,根本違反國際規範。他說,國產疫苗是戰略物資,但政治不應凌駕專業,科學東西絕不能用政治手段解決!他批評,免疫橋接根本不是美國食藥局(FDA)或是歐盟藥政機關認可的技術,在全世界都沒有類似案例,用免疫橋接檢驗中和抗體,並不等於免疫保護力,免疫橋接也不能取代第3期試驗,政府如果要給予高端疫苗緊急授權,應依據國際標準,要求高端至少提出第3期期中報告,才能審查緊急授權申請。郝龍斌委任的律師葉慶元也說,向行政法院聲請停止執行挑戰很高,因為行政法院過去在環保案件,一向對於利害關係做較寬鬆認定,允許人民針對環境影響評估等處分進行訴訟。但相對於環保訴訟,高端疫苗的緊急授權處分,對公民的傷害更為立即、直接,依照「舉輕以明重」的法理,更應符合利害關係要件。他強調,高端疫苗緊急授權過程疑點重重,不僅審查程序有瑕疵,核發緊急授權的要件也與法律不符,絕對有停止執行的必要。

WHO:印度變異株Delta已成全球主流病毒株 台灣5例境外移入個案檢出
世界衛生組織(WHO)昨宣布,傳播力較強的印度變異株(Delta)正式成為全球傳染主流。對此,中央流行疫情指揮中心指揮官陳時中說,不管是什麼變種病毒,都需要非常提高警覺,若檢驗到,精準疫調、快速的封鎖是需要來做的。醫療應變組副組長羅一鈞表示,去年10月至今,國內共完成278案定序,最多是英國變異株,有199案,而南非、巴西變異株分別是6案和4案。另有桃園醫院的加州變異株19案,菲律賓P3變異株2案。印度變異株目前為止有5案,分別是案1117、1144、1382、1192、1215都有印度旅遊史和居住史,另有1人是烏茲別克的旅遊史,本土個案還沒有印度變異株。羅一鈞表示,在英國病例中,有9成個案感染印度變異株,大部分都是感染到沒打疫苗,或只有打1劑疫苗的人,印度變異株會增加家戶感染、住院比率,因此當地提出警告,呼籲民眾儘快完成2劑疫苗的接種。印度變異株的預防,需要的是2劑的疫苗接種。對於是否會需要更長的隔離時間來防堵印度株,羅一鈞表示,目前沒有證據說印度變異株比英國變異株潛伏期長,拉長隔離期沒有科學上的佐證。印度株的預防方式沒有不同,不管什麼變異株,只打1劑的效果都不足。對於預防住院,不管是AZ、BNT,接種2劑,都可以達到9成以上的效果,提醒民眾儘速接種。

世衛宣布Delta成全球傳染主流 羅一鈞:本土尚未出現印度變異株個案
世界衛生組織(WHO)昨宣布,傳播力較強的印度變異株(Delta)正式成為全球傳染主流。對此,中央流行疫情指揮中心指揮官陳時中說,不管是什麼變種病毒,都需要非常提高警覺,若檢驗到,精準疫調、快速的封鎖是需要來做的。醫療應變組副組長羅一鈞表示,去年10月至今,國內共完成278案定序,最多是英國變異株,有199案,而南非、巴西變異株分別是6案和4案。另有桃園醫院的加州變異株19案,菲律賓P3變異株2案。印度變異株目前為止有5案,分別是案1117、1144、1382、1192、1215都有印度旅遊史和居住史,另有1人是烏茲別克的旅遊史,本土個案還沒有印度變異株。羅一鈞表示,在英國病例中,有9成個案感染印度變異株,大部分都是感染到沒打疫苗,或只有打1劑疫苗的人,印度變異株會增加家戶感染、住院比率,因此當地提出警告,呼籲民眾儘快完成2劑疫苗的接種。印度變異株的預防,需要的是2劑的疫苗接種。對於是否會需要更長的隔離時間來防堵印度株,羅一鈞表示,目前沒有證據說印度變異株比英國變異株潛伏期長,拉長隔離期沒有科學上的佐證。印度株的預防方式沒有不同,不管什麼變異株,只打1劑的效果都不足。對於預防住院,不管是AZ、BNT,接種2劑,都可以達到9成以上的效果,提醒民眾儘速接種。

AZ疫苗效果有限?印度株入侵全球 專家:台灣須提前部署
全球新冠肺炎疫情延燒,不少國家都遭變種病毒侵襲,其中最常見的是英國變異株,不過專家擔憂,目前印度變異株也開始往全球入侵,在大洋洲、非洲、亞洲和少部分的歐洲都有發現。由於傳播力強,加上疫苗對其效果有限,憂釀全球大流行,專家呼籲台灣要提前部署、強烈注意。台大公衛學院教授陳秀熙表示,全球變種病毒走的速度非常快,其中最多的是英國株,印度株也慢慢入侵,大洋洲佔比為31%、亞洲為26%、非洲12%、歐洲7%、北美洲5%、南美洲3%。以英國波爾頓為例,AZ疫苗對印度株的效果是個挑戰。在日本東京,也同樣受印度株影響。陳秀熙表示,印度株傳播力非常強,全球會不會重新開始印度株大流行,令他擔憂。面對印度株,台灣必須提前部署,針對病毒基因作分析。除境外管制,對於印度株的擴散也需強烈注意。另對近期的本土疫情,陳秀熙說,萬華茶館事件剛擴大時,全國實施非藥物公衛措施(NPI),落實度僅46%,導致隱性傳播不斷發生,隨著警戒升級,國人的落實度已升至75%,雖可讓流行有所趨緩,換取等待疫苗的時間,但仍會不斷有個案出現,醫療量能將受到很大挑戰,最好能確實做到3級警戒要求,避免群聚,管好傳統市場、特種行業等,讓NPI措施做到90%,如此一來,推估到了6月中旬,疫情就能受控制。

英國變種再變種!印度變種病毒可能主宰世界第三波疫情 現有疫苗難敵
印度新冠疫情失控,近期單日新增確診數突破40萬人,據世界衛生組織(WHO)表示,印度變種病毒「B.1.617.2」是疫情持續惡化的原因之一,國內專家表示,這種印度變異病毒株是英國變種病毒的再變種,本身傳播力已較強,另又與南非、巴西變異株類似,都有484位點的變異,容易逃脫疫苗的保護,恐讓現有疫苗保護力僅剩10%至25%,也可能導致第三波疫情!印度新冠疫情失控,可能導致第三波疫情!(圖/達志/美聯社)「B.1.617.2」變異病毒株是在去年10月首次被發現,據世衛首席科學家斯瓦米納坦(Soumya Swaminathan)接受《法新社》受訪時表示,以目前在印度觀察到的狀況,證明這是一個迅速擴散的變異株,也是印度疫情急遽惡化的主要兇手之一。英國英格蘭公共衛生署(PHE)也將印度發現的「B.1.617.2」變異病毒株,列入「引發疑慮變種」的名單,確定印度變種株已演變為主流的變異株之一,也可能會讓全世界進入第三波疫情。印度變異株將使原本疫苗的保護力僅剩下10%至25%。(圖/達志/美聯社)根據《蘋果新聞網》引述長庚大學新興病毒感染研究中心主任施信如的看法出,「B.1.617.2」變異病毒株,是來自英國的B.1.1.7變異株的變異,但不同的是已經出現抗原性的位點改變,會逃脫疫苗的保護,這是非常嚴重的。施信如表示,這種突變的位置,改變了抗原性,會讓身體產生的抗體,對新變種病毒株的結合能力變不足,進而讓疫苗阻斷病毒的能力變弱。將來各國施打疫苗,可能得考慮「雞尾酒」打法。(圖/達志/美聯社)由於目前尚無針對印度株保護力的人體實驗,但以實驗室研究推估,印度變異株將使原本疫苗的保護力僅剩下10%至25%;但施信如認為,這不代表疫苗的保護力完全消失。施信如表示,以過去流感疫苗的研究發現,當多數疫苗改為新的特定位點後,有可能流行的病毒株位點又變回舊的版本,將來各國施打疫苗,可能得考慮「雞尾酒」打法,而這也意味著病毒已經不會消失,朝流感化發展,人類將來都得與之共處。據中央疫情指揮中心發言人莊人祥10日下午表示,印度變種病毒目前傳到很多國家,至於打疫苗模式,若確定目前的疫苗無效,可以考慮是否以新的疫苗或原有疫苗多打幾次,另外雞尾酒疫苗也得等將來上市疫苗,有能夠針對印度株的產品問世,目前還沒辦法使用雞尾酒疫苗的模式。