單劑型
」 疫苗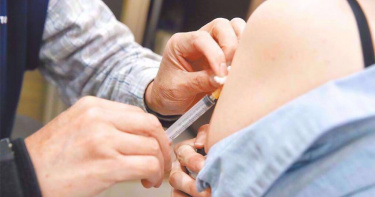
花蓮光復災區外傷激增 國光、安特羅急送5千劑破傷風疫苗
為支援花蓮光復鄉災區需求,國光生技集團(4142)宣布,與疾管署、花蓮縣衛生局聯絡,30日急送5千劑破傷風疫苗到花蓮,為災民及全台湧入救災的鏟子超人們,提供外傷後必打的破傷風疫苗,避免遭汙泥中的異物刺傷造成感染,一同支援花蓮災區重建家園。近日花蓮光復鄉災區正極力清淤,災民以及來自台灣各地志工為協助清理家園,遭厚泥中暗藏的鐵釘、玻璃碎片、鐵片、樹枝等物刺傷,雖穿著厚底雨鞋,仍有不少人被刺到腳底受傷、鮮血直流,災區外傷傷患逐步增加。根據花蓮慈濟醫院的統計,9月24至28日已經診治502名外傷傷患,破傷風疫苗是目前災區急需的醫藥資源。國光生技與安特羅生技在第一時間主動接洽疾管署及花蓮縣衛生局,除了配合衛福部流感疫苗花蓮災區優先接種的政策外,也主動表達捐贈破傷風疫苗意願,衛生局表示破傷風疫苗為災民及時所需的醫療物資,國光及安特羅已依災區需求,緊急配送流感疫苗並追加捐贈5千劑破傷風疫苗今日送達,全力支援災區。若後續災區還有其他疫苗需求,將全力捐助,善盡國產疫苗廠的社會責任,與全台民眾一同守護災民。破傷風疫苗可預防破傷風桿菌感染引發肌肉僵硬、抽搐等神經重症,尤其外傷、車禍、外科手術患者或孕婦,接種破傷風疫苗被視為最有效的預防方法。國光生技指出,國光破傷風類毒素是唯一取得藥證的國產破傷風疫苗,每年至少可穩定供應100萬劑,滿足疫苗自給自足的目標。國光破傷風疫苗除了在地自主生產、供貨穩定外,國光生技也持續精進在劑型上升級改良,由於現行破傷風疫苗多為瓶裝或安瓶裝,國光開發單劑型針劑,可縮減開瓶抽取步驟,更方便急診及臨床醫師使用,單劑型破傷風疫苗預計今年底全面供貨,提供更符合第一線緊急使用需求的疫苗。

披衣菌肆虐無尾熊族群 澳洲批准全球首款「專用疫苗」救命
澳洲國寶無尾熊正陷入前所未有的生存危機,原因就是長年肆虐的披衣菌(chlamydia),這不僅造成無尾熊的失明與不孕,甚至導致大批死亡,而最新的研究突破為牠們帶來希望。澳洲聯邦監管機構已批准全球首支專為無尾熊研發的披衣菌疫苗。這項成果來自陽光海岸大學(University of the Sunshine Coast, UniSC)團隊超過十年的努力。根據《BBC》報導微生物學專家廷姆斯(Peter Timms)博士指出,部分野生族群感染率高達70%,族群數量逐步逼近滅絕邊緣。不同於人類菌株,這種細菌能透過交配、親密接觸,甚至幼崽在母親育兒袋內餵食時傳播。傳統抗生素治療雖能控制病情,卻會破壞無尾熊消化桉樹葉的能力,反而引發飢餓與死亡,使疫苗成為唯一可行的長期解方。這款單劑型疫苗無須追加劑,臨床試驗證實能顯著降低繁殖年齡無尾熊的發病率,死亡率至少下降65%。研究主導者菲利普斯(Sam Phillips)博士表示,這是針對野生無尾熊規模最大、持續時間最長的研究,成果已為全國推廣奠定基礎。團隊下一步希望獲得更多資金,讓疫苗能在各地野生動物醫院與獸醫診所廣泛使用。保育人士早已將披衣菌視為「無尾熊頭號殺手」。現存野外個體數估計僅剩5萬隻,加上土地開發、乾旱與叢林大火,生存壓力更為嚴峻。雄雌個體均可能遭感染,發病後常伴隨泌尿道感染、結膜炎與失明,痛苦難以形容。許多野生動物醫師坦言,每天仍有不少隻無尾熊因病痛或失能而被迫安樂死,疫苗問世或許是避免滅絕的最後防線。疫苗的批准時機,更與保育政策相互呼應。就在新南威爾斯(New South Wales)政府宣布劃設17.6萬公頃州立森林,打造「大無尾熊國家公園」(Great Koala National Park)的隔天,疫苗通過的消息再度振奮人心。該公園預計能保護超過1.2萬隻無尾熊,並為100多種受威脅物種提供棲息地。環境部長潘妮・夏普(Penny Sharpe)強調,新公園的成立將確保無尾熊能存活至未來,讓後代仍能在野外見到牠們。對澳洲來說,這是一場與時間競賽。疫苗不僅是科研突破,更是野生族群延續的轉機。當科學與政策攜手,無尾熊或許真的能逃過「瀕絕」的命運。
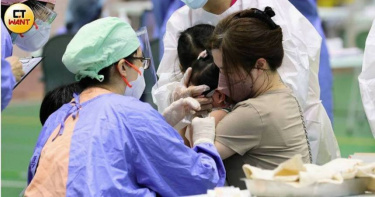
JN.1疫苗10月起開打!疾管署揭「沒買最新款」原因 接種時程出爐
疾病管制署(下稱疾管署)今(10日)表示,世界衛生組織(WHO)於今年4月針對COVID-19疫苗抗原組成建議使用單價JN.1作為新疫苗抗原成分,以提升對抗主流病毒株之免疫保護力;另歐盟與鄰近日本、韓國亦同時採用單價JN.1疫苗。目前國內外疫情仍以JN.1為主流病毒株,考量KP.2及KP.3變異株為JN.1衍生後代,且兩者與JN.1之間棘蛋白突變位點差異小,經昨(9日)提案衛生福利部傳染病防治諮詢會預防接種組(ACIP)討論,建議以單價JN.1疫苗因應我國今年秋冬面臨COVID-19之疫情,儘早提供民眾接種提升免疫保護力,防範新冠侵襲。疾管署說明,另經參依美國CDC針對COVID-19疫苗與流感疫苗同時接種之安全性,考量併同接種可提升接種率,降低併發COVID-19及流感重症發生風險。因此,今年10月1日起單價JN.1疫苗將與流感疫苗同步分兩階段開打。由於今年秋冬供應之莫德納疫苗12歲以上為單劑型(0.5mL/劑),12歲以下為多劑型(0.25mL/劑/每瓶10劑),相關接種期程及建議如下:一、接種時程與對象:(一)第一階段(今年10月1日起):同流感疫苗第一階段實施對象。(二)第二階段(今年11月1日起):滿6個月以上民眾(未列在第一階段實施對象)。二、接種建議:(一)滿6個月至4歲幼兒:1.未曾接種COVID-19疫苗者接種2劑,2劑間隔4週(28天)以上;2.曾接種COVID-19疫苗者接種1劑,與前1劑間隔12週(84天)以上。(二)滿5歲以上兒童、青少年及成人:接種1劑,曾接種COVID-19疫苗者與前1劑間隔12週(84天)以上。疾管署說明,後續將依疫苗進口期程再另行公布相關接種規劃資訊,以提供國人接種,增進免疫保護力,降低重症及死亡風險。

新冠疫情時代 小小孩18個月得挨20針
在疫情時代我們經歷了1、2、3…以及看似無止盡的追加劑,有小兒科醫師精算嬰兒出生到1歲6個月間,常規疫苗+流感+新冠要至少挨超過20針,尤如針線包;2020年台灣再度引進6合1疫苗,整合嬰6個月大常規5合1(白喉、百日咳、破傷風、小兒麻痺、嗜血桿菌)疫苗及B肝疫苗,不少家長選寧可自費接種,也免去一次面對寶貝撕心裂肺的拒針戲碼。小兒科醫師施勝桓指出,嬰兒出生至1歲6個月,常規疫苗需要注射的就有16針,再加上流感疫苗以及新冠疫苗,總共超過20針,現今多雙薪家庭,不少家長為帶嬰兒依規定時間接種疫苗需頻繁請假,相當不便,且多注射一劑就多一次疫苗引起副作用的風險,尤其不少小孩因疼痛對針劑恐懼,經常在診間上演撕心裂肺、四肢劇烈掙脫的劇碼。六合一疫苗是把嬰兒六個月大的時候必須接受的五合一疫苗以及B型肝炎疫苗兩劑整合為一劑。過去台灣曾短暫引進6合1疫苗做為公費施打,2018年因國際B肝疫苗供需失衡再恢復為5合1疫苗,2020年台灣再度引進6合1疫苗,供家長選擇可自費接種。施勝桓指出,6合1疫苗的優點除讓6個月的嬰兒少打1劑,臨床也發現昔日公費、單劑型B肝疫苗,20%的接種者在國中例行性的健康檢查中已偵測不到B肝的抗體或者是B肝抗體不足,需再自費接種B肝疫苗,採6合1疫苗抗體增強22倍,可減少小朋友成長後補追加B肝疫苗的機率,這也是不少家長考量讓寶貝在6個月大時棄公費5合1改接種6合一的原因。

「嬌生單劑型疫苗」抗體較莫德納低 美專家建議政府追打第2劑
為對抗新冠肺炎疫情,各國公衛專家關注如何讓疫苗效力更強、更久,美國食品暨藥物管理局(FDA)外部顧問15日建議FDA批准,所有接種嬌生COVID-19「單劑型疫苗」的人接種第2劑疫苗。綜合「路透社」等外媒報導,食藥局的疫苗和相關生物產品諮詢委員會(Vaccines and Related Biological Products Advisory Committee)支持所有接種嬌生(Johnson & Johnson)疫苗的18歲以上民眾,可在接種第1劑疫苗後,至少2個月後接種追加劑,小組成員指出,相較於莫德納疫苗、BNT疫苗這類mRNA疫苗而言,嬌生疫苗產生的抗體濃度較低,因此給出上述建議,雖然這類建議無強制力,但FDA一般都會遵守。會議主持密西根大學公共衛生學院流行病學者孟多(Arnold Monto)表示,「這是公衛上的當務之急,我們看到一群人整體疫苗效力較低,迫切需要做些什麼」。報導指出,一但美國食藥署批准施打第2劑,疾病管制暨預防中心(CDC)就會因應接種的群體提出具體建議,而美國疾管中心也預定下週開會討論追加劑議題。事實上,為確保脆弱人群有足夠保護力,美國食藥局在上個月就批准65歲以上、重症高風險人群,和工作上易接觸病毒者追加施打輝瑞/BNT疫苗,目前也正在考慮將接種疫苗追加劑的年齡下降到40歲。
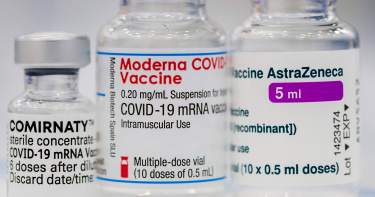
11月起沒打疫苗不得入境 美國CDC「WHO、FDA授權疫苗均可」
美國白宮於20日發布聲明,表示從11月起,外國成年旅客必須「完整接種」疫苗後方可入境美國。美國疾病管制與預防中心(CDC)則表示,只要是美國食品藥品監督管理局(FDA)與世界衛生組織(WHO)授權獲批准的疫苗都可以,但目前待認可的名單目前還在討論中。綜合外媒報導指出,目前美國食品藥品監督管理局所核准的疫苗,分別是莫德納(Moderna)、輝瑞Pfizer/BNT與嬌生疫苗(單劑型)等3種疫苗。而英國藥廠阿斯特捷利康(AstraZeneca)的AZ疫苗、中國科興(CoronaVac)與國藥(Sinopharm)疫苗、俄羅斯的「史普尼克五號」(Sputnik V)均尚未通過FDA的認可。至於世界衛生組織方面,目前WHO已經核可了7種疫苗,除了莫德納(Moderna)、輝瑞/BNT與嬌生疫苗(單劑型)外,另外還有AZ疫苗、中國科興(CoronaVac)與國藥(Sinopharm)疫苗與有著「印度版AZ」稱號的Covishield等7種疫苗,而俄羅斯的「史普尼克五號」也不在WHO的核可範圍內。美國CDC發言人諾德隆德(Kristen Nordlund)表示,CDC目前認為,完整接種FDA或WHO所授權、核准的疫苗,其實就可以符合美國政府所要求的入境標準。但目前對於實際要核可那些疫苗,目前尚無定論。而目前除了已知該政策將於11月初上路外,其餘相關細節也均未公布。
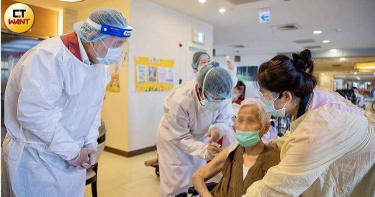
AZ爽約率8%!醫憂「高端」恐更多 陳時中回應了
國內疫苗持續施接種,第六輪高端疫苗將於明(23日)開打,共有59萬9613人完成預約,距離其提供的61.4萬劑,尚有1.5萬劑未預約。中央流行疫情指揮中心宣布8月16日下午2點後新登記或加選意願為高端疫苗者,可在23日早上10點至24日晚上6點預約接種,不過有醫師擔心爽約率會增加,對此,陳時中也回應了。媒體詢問,過去AZ和莫德納都有爽約的情況,如果很多民眾預約卻不來打,那些疫苗該怎麼辦?陳時中表示,會將數量給估進去,到時侯會看看,如果真的很多,可能會再開放預約,強調8月23日至29日地方施打量能沒問題,「有疫苗、有人想要打,那我們就會再開」。陳時中透露各廠牌疫苗爽約率約5%。(圖/翻攝自衛福部直播)另外,有現場協助疫苗施打的醫師指出,AZ爽約率大概是8%,莫德納的爽約率不到2%,怎麼看高端疫苗的預約狀況?陳時中解釋,高端並不是以打殘劑為目標,目前提供200萬劑是單劑型,後面才是多劑型,「不會有抽到最後有剩下,滿完整的」,出錯機會也比較小。至於爽約率,根據統計資料,疫苗爽約率大約5%,「並沒有廠牌上的差異」,高端會有多少人爽約,要等打完才會知道。據了解,苗栗縣議會日前通過提案,建議苗栗施打的疫苗須經過「國際認證」,對此陳時中表示,「疫苗接種屬全國統一事項,需依照中央規定辦理」,因此會按照預約施打,不受影響。