GMP藥廠
」
台灣大塚製藥歡慶50周年 展望全齡化健康未來
台灣大塚製藥在台成立屆滿50周年,日前於慶祝活動上邀請來政務委員陳時中、桃園市衛生局局長賈蔚等人到場祝賀,大塚控股代表取締役會長大塚一郎、取締役副社長松尾嘉朗、大塚製藥常務取締役坂東幹夫,與大塚製藥工廠取締役岡田達明等人也特別自日本前來共襄盛舉,現場十分熱鬧。台灣大塚製藥總經理松尾政志於活動上表示,大塚製藥的抱負是秉持「貢獻人類健康與福祉」核心理念,持續深耕台灣,放眼下一個50年的發展。企業斥資赴海外設廠,是展現有意長期在地深耕,穩定經營的決心。台灣大塚製藥董事長許信義致詞表示,自1974年成立以來,即在桃園中壢工業區投資建設工廠,以提升產品品質,迅速滿足當地患者需求為首要目標,並於2010年獲得PIC/S GMP藥廠認證,2018年更斥資數億元興建軟袋工廠,持續透過優質產品建立口碑,為台灣醫療與患者提供卓越的健康產品。50年來的卓越成果與新世代目標台灣大塚製藥的業務最初以輸液產品為主,並與台大醫院合作研發營養輸液系列,此創新在台灣醫療界廣受好評與認可。50年來,台灣大塚製藥逐步擴展至治療藥品、營養品及消費者產品等多個領域,持續為人類健康保障做出貢獻。總經理松尾政志表示,公司致力於實現「全方位健康」的目標,從出生、成年到老年,提供各階段所需的健康支持,甚至當台灣醫療界及民眾需要緊急支援時,也樂於能盡份心力協助,期許在台穩紮穩打不斷前進,成為百年企業。克服少子高齡化與個別化的醫療挑戰針對台灣少子高齡化的社會趨勢,台灣大塚製藥未來將引進更多符合高齡社會需求的健康產品。松尾政志指出,集團正在研發新的個別化醫療技術,致力於克服疾病,並持續探索創新的診斷與治療方法。未來,台灣大塚製藥將推動數位化健康解決方案,並利用AI技術進一步提升產品與服務的精準度與效率。AI技術融入醫療 跨界合作創新健康價值松尾政志稱2024年為台灣大塚製藥「AI元年」,並透露目前正與AI軟體公司合作,針對臨床需求提供更具效率的數據分析。過去50年累積的大量臨床資料,將透過AI技術更完善地應用於醫療系統,為臨床診斷與治療提供參考,並進一步提升產品開發與應用的效率。未來,台灣大塚製藥計劃導入更多數位應用產品,特別是針對精神科診斷與治療的電子化產品。隨著總公司逐步擴展至全世界31個地區,台灣大塚製藥將與全球合作夥伴共同推動全方位健康解決方案,打造一個更健康的未來。家族傳承與台灣深厚連結 邁向百年企業大塚集團現任會長大塚一郎,從公司創立以來造訪台灣多次,展現對台灣市場的高度重視與支持。他在晚宴致詞中特別提到,很開心能在日本以外的地區,發展輸液業務,與台灣合作夥伴有著許多美好回憶,未來台灣大塚製藥將延續此深厚合作,並不斷創新與發展,繼續為台灣的醫療與健康產業帶來更多貢獻。松尾政志在50週年活動現場感性表示,很謝謝台灣同仁們的努力付出,與公司一同並肩前行,強調台灣大塚製藥將秉持初心,積極應對未來的挑戰,邁向下個50年的全新里程,力爭成為百年長青企業。台灣大塚製藥計劃未來導入更多數位應用產品,特別是針對精神科診斷與治療的電子化產品,將與全球合作夥伴共同推動全方位健康解決方案(圖/台灣大塚製藥提供)。

憂「熱原反應」害命 羅廷瑋疾呼進口食鹽水別便宜行事
台灣生理食鹽水大缺貨,衛福部緊急從越南、馬來西亞採購食鹽水進口,宣稱進口食鹽水都符合國際藥品品質PIC/S標準,但是立委羅廷瑋在立院質詢時卻踢爆,衛福部日前進口一批非PIC/S標準會員國的越南食鹽水,照理說食藥署專案進口前應該要先查廠,才能確保品質安全,但衛福部迄今無法提出查廠證明。據指出,由於羅廷瑋的質詢當場「考倒」行政院長卓榮泰、衛福部長邱泰源,引發政院高度關切。食藥署次長林靜儀昨晚在臉書發文回應,指越南雖非PIC/S組織會員國,但該批食鹽水是委託「在台日商」進口、該越南藥廠也通過日本醫藥品醫療機器綜合機構(PMDA)認證,PMDA也是PIC/S組織會員。對此,羅廷瑋今天再開記者會,直指生理食鹽水要打入人體、過去國內也有食鹽水品質出問題、引發病患感染前例,衛福部應該要照規定辦理,不應便宜行事。羅廷瑋指出,衛福部堅持認為,日本醫藥品醫療機器綜合機構(PMDA)曾對該越南廠進行查核,而且也看到書面文件,就替品質掛保證,因為日本極東製藥也是日本PMDA查核認定的GMP藥廠,但日本極東製藥卻數據造假,欺騙日本政府長達30年。何況,日本查核與衛福部查廠有何關係?如果日本查核過關、書審就能進口,那麼其他50幾個PIC/S組織會員國的藥廠產品,是否也可以比照「不需衛福部查廠就可直接進口」?羅廷瑋所指的日本製藥公司「極東」,是國人耳熟能詳的胃腸藥「正露丸」製造藥廠,日本富山縣政府今年初查獲,極東製造的「正露丸」在所需必要成分不足下,提出造假的藥品試驗結果後出貨,而且長達多年,讓向來自豪藥品品質的日本輿論高度震驚。此外,針對林靜儀坦承專案進口食鹽水因缺乏藥證,如果患者注射後出問題「不適用藥害救濟」,食藥署長莊聲宏下午也緊急出面說明,即使不適用要害救濟,進口食鹽水應該可以引用「消保法」向進口藥廠求償。不過,羅廷瑋質疑,專案進口的生理食鹽水,未經我國政府查廠、未取得我國藥品許可證,食藥署長居然還說可用「消保法」去求償,衛福部確定這樣的作法可行嗎?他痛批人民恐無法接受。2015年北榮曾爆發院內不明感染事件,讓北榮醫護倍感壓力,院方反覆清查後,才發現是使用到被污染的永豐生理食鹽水注射液,圖為北榮當時大動作召開記者會自清並說明調查過程。(圖/報系資料照)羅廷瑋也提醒衛福部,食鹽水雖是很常見的藥品,但只要滅菌不完全,產品內有熱原(pyrogen),患者恐產生熱原反應,嚴重者可能危及病患生命安全,否則,衛福部為何要求國內合法認證GMP藥廠全程無菌操作製造?永豐為何又被勒令停廠?衛福部絕對不能便宜行事,將責任推給進口藥廠、以及要求醫護「加強監控」。中華民國基層藥師協會沈采穎表示,他曾多次疾呼,衛福部應立即提供醫療院所「出現問題的永豐生理食鹽水批號」,醫療院所醫護人員才能加強監控,在第一時間查獲可能有疑慮的食鹽水、不要危及病患健康。她說,2015年,台北榮總爆發院內感染事件,當時外界懷疑榮總內部控管失當,但榮總自認內控絕無問題,榮總只好將醫院上下「全翻過一遍」,最後才發現是使用永豐遭污染生理食鹽水注射液,導致病患感染皮氏羅爾斯頓氏菌(ralstonia pickettii),立即停用該批食鹽水。沈采穎指出,榮總幸運的是,因為院內有感染科,有能力查明院內不明感染原因,但未必每一家台灣的大小醫療院所都有此能力,衛福部若不提供有問題的食鹽水批號,現在又逕自放行非PIC/S會員國藥廠的產品進口,萬一出問題,患者還不能申請要害救濟,也難怪衛福部官員雖然不斷口頭「保證」,但應該要提出更具體的說明及因應方案,才能讓患者家屬、醫護人員放心。
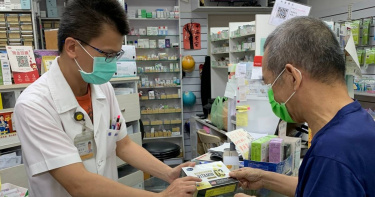
「活性維生素D」攝取過量傷健康 2方式辨識防吃錯
維生素D近來成為熱門話題,主要是有研究顯示,過去認為多多攝取維生素D有助身體整體健康,但根據小鼠研究測試,發現患有阿茲海默症的老鼠攝取維生素D後,大腦狀況反而更惡化。日前也有婦人未留意而攝取過量活性維生素 D,造成高血鈣心律不整,經醫師緊急處置,停用和補充大量水分後,症狀才獲得緩解。近來受COVID-19 疫情影響,民眾對防疫期間要如何增強體能和身體保護力, 都會特別關注留意,其中維生素D更是最常被提到需補充攝取的維生素之一。但維生素D有分「活性」、「非活性」兩種,很多民眾並不清楚其中的差別。上圖為非活性維生素D,下圖則為活性維生素D,會有藥物許可證字號。(圖/南投縣衛生局提供)南投市和康藥局林宏益藥師說,維生素D是人體維持基礎健康的一種脂溶性 維生素,分為活性、非活性2種,活性維生素D為處方用藥,除特殊情形(如洗腎病人)需補充,一般人僅需補充非活性維生素D。非活性維他命除透過曬太陽來自行合成以外,也可以透過食物來獲得,市售的維生素D以D3為主,提醒民眾注意購買活性維生素D應在醫師診療指示下服用,也可以請教社區藥局的藥師,都可獲得正確的藥事諮詢建議。 林宏益藥師說民眾自行購買維生素D有2個簡單判斷活性與非活性的方法, 非活性維生素D的單位是「ug」或是「IU」;活性維生素D的單位是「ug」(活性不會用IU表示)且會有藥物許可證字號。一般民眾每日建議攝取量為800~2000IU,請注意勿攝取過量。南投縣衛生局提醒民眾,現行法規規定,維生素D依產品標示或仿單,若每日食用劑量若超過 800IU,即列屬藥品管理,選購時請至藥局或販賣業藥商購買,並選擇USP或GMP藥廠製造或是有認證標示的產品,此外產品上需標示客服電話,讓消費者可以得到專業諮詢服務。另呼籲民眾針對劑量超過 800IU 維生素D除自用外,切勿透過社群網路轉售,以免違反藥事法相關規定受罰。

清冠自費幕後2/憂指揮中心解散清冠EUA失效 藥界籲及早因應
防疫指揮中心本週將與國內中醫、中藥界開會,討論是否限縮「公費」清冠一號給藥對象,新方案最快八月實施,引發議論。藥界人士則提醒,因目前國內中藥成藥只有「經典方」能在取得GMP認證後上市販售,但「清冠一號」是新方,目前雖暫時取得緊急授權(EUA),但想取得藥證上市販售,仍須完成一到四期完整實驗,而清冠一號目前僅做了第一期實驗。藥界因此擔憂若指揮中心未來解散,清冠一號EUA也可能也同步面臨失效,民眾短期內恐難再拿到新冠一號,建議指揮中心及早因應。中華民國防疫學會理事長王任賢指出,雖藥界擔心的問題應該不至於發生,但若藥界有此疑慮,指揮中心應在公布公費清冠一號使用對象檢討案時,一併說明,讓業者及民眾安心。他認為,因為清冠一號雖是取得指揮中心EUA才能上市,但EUA核發單位是衛生部食藥署,即使指揮中心未來不復存在,清冠一號EUA應還是有效。清冠一號是國家中醫藥研究所在2020年開發、用於治療新冠肺炎的中藥新處方。該藥方是依據明代「攝生眾妙方」所輯的「荊防敗毒散」方子,再搭配清熱解毒藥材研究改良,並在2021 年 5 月獲得國內臨時藥品許可證(EUA)上市。清冠一號上市後,先在各大醫院經由中醫會診,針對住院中、重症患者投藥,當時第一批獲准生產有八家國內藥廠,稍後並提供外銷。今年 4 月16日,本土案例突然直線上升,為強化輕重症分流收治,確保醫療量能及病人即時獲得醫療照護,指揮中心在朝野立委要求下,宣布開放清冠一號給 PCR 陽性確診個案及需居家照護者,經視訊診療評估後開立公費使用,防疫指揮官陳時中當時還曾盛讚「新冠一號」是台灣之光,而國家中醫藥藥研究所所長蘇奕彰則說明,根據研究結果顯示,清冠一號除對抵抗新冠變異株有效外,在中重症的預防或改善也有效果。衛福部國家中醫藥研究所所長蘇奕彰表示,「清冠一號」不僅實際運用於臨床治療,經過研究,還可多靶點治療新冠肺炎,且有效預防輕中症轉為重症、死亡發生。(圖/翻攝自紀惠容臉書)「勝昌也被授權出品清冠一號,銷路原本普通,但在4月16日後,詢問者突然暴增,原本參與生產的八家藥廠存貨供不應求,甚至來不及生產,衛福部後來又緊急開放六家藥廠參與製作」,國內老牌GMP藥廠「勝昌製藥」總經理李威著回憶。李威著解釋,清冠一號藥方有10味中藥材,只有桑葉、薄荷、魚腥草台灣能生產,其它七項藥材都需從大陸進口,因為台灣清冠一號熱銷,帶動全球銷量也提升。以其中台灣未生產的藥材「栝樓實」為例,四月下旬成本就從每公斤150元、漲價到800元,並帶動產地、大陸河南河北藥材同步上漲。李威著說明,中國大陸主要對治新冠肺炎中藥方以「清冠排毒湯」及「蓮花清瘟飲」為主,給藥思路與「清冠一號」不同,再加上大陸各省各有不同的中藥指引。相較下,「清冠一號」等於是靠著衛福部EUA闖出名號,這也是台灣中藥界首度讓民眾瞭解,中醫藥能與時俱進,有效對抗最新傳染病。但清冠一號熱銷,卻也凸顯國內中醫界與中藥界長期以來遭遇的瓶頸,包括國際學術論文報告篇數不如西藥多、遭到西醫藥界質疑,非傳統「經典方」新藥想上市,得比照西藥、進行嚴格四階段實驗,更別說現行健保給付中,中醫藥原本就僅佔5%,面對「西醫藥」主導的準制,中醫藥原本在台灣醫藥結構中就是少數,也很弱勢。也獲得授權生產清冠一號的「勝昌製藥」總經理李威著表示,「清冠一號」是靠著衛福部EUA闖出名號,也是台灣中藥界首度讓民眾瞭解,中醫藥能與時俱進,有效對抗最新傳染病。(圖/翻攝自勝昌製藥臉書)反觀中國大陸,近年逐步摒棄過去用西醫藥模式發展中醫藥的作法,推出包括老中醫師徒制、中藥臨床試驗、論文投稿點數計算改採符合傳統中醫邏輯進行,雖然這些新制度能否成功還很難說,但卻讓兩岸中醫界看到另種新可能性。「清冠一號藥理機轉其實與西藥抗病毒藥物類似,且具有副作用相對輕微(安全性較高)、取得容易、費用比抗病毒西藥低等優點,適合大型疫病來襲時大量備藥」,率先呼籲政府將清冠一號納入公費給付的藥師沈采穎認為,清冠一號讓外界看見中醫與中藥價值,建議政府應在清冠一號的基礎上「趁勝追擊」,增加中醫預算,並針對包括清冠一號、清冠二號等中藥方進行臨床效能驗證,努力發展本地中藥材,讓中醫藥與西醫藥分進合擊,協助台灣通過後新冠時代的疫情考驗。

民眾瘋搶清冠一號 中醫師警告:沒染疫服用反導致免疫出問題
近期由於本土疫情升溫,不少民眾開始搶購快篩以及可以治療疫病的「清冠一號」。為此,中醫師強調,清冠一號並不是保健方,沒感染新冠肺炎的話吃了也沒用,反而會讓免疫系統出問題。而就算是確診患者,此藥也並非適合每個患者,因此呼籲民眾無須搶購清冠一號,或是與清冠一號相同藥方的複製品。根據媒體報導指出,對於民眾搶購清冠一號複製方藥品,甚至服用來「預防」新冠肺炎等事情,台灣中醫藥教育學會理事長黃建榮表示,「清冠一號不是保健方,沒染疫也吃是不正確的觀念,藥材非常珍貴,以預防為名把藥材都用完,等到真生病時也許就沒藥了!」長庚體系中醫醫療發展召集人黃澤宏受訪時表示,清冠一號的藥方先前曾公開,是由10味清熱解毒藥方組成,但由於每個人體質不同,清冠一號未必能適用於每位患者,因此應該回歸最基本面,由中醫師根據患者症狀、體質來進行配藥。也因為公開藥方的關係,清冠肺炎的「坊間複製方」有水煎劑、濃縮藥粉、生藥材打成粉末3種版本。其中水煎劑如果使用合格藥材,效果會比較接近GMP藥廠生產的版本,另外兩種版本會根據配方比例有不同的交互作用,因此很難有實證。
食藥署公布杏輝藥品等3藥廠 「嚴重違反GMP」
食藥署在官方網站最新公告三家藥商嚴重違反GMP(藥品優良製造作業規範),其中杏輝藥品有多達20款藥物出問題、需下架回收,被食藥署盯上;杏輝也提交報告給食藥署說明原因。根據《自由時報》報導,杏輝藥品公司上月因多項藥物有持續安定性試驗不合格等問題,需下架回收多達20款藥物,世達藥品公司也有藥品製程異常而下架13藥品,至於博謙生技公司則有原料藥的無菌模擬充填試驗結果造假,被食藥署公告為「嚴重違反GMP藥商」。杏輝藥品公司。(圖/翻攝自杏輝醫藥集團網頁)據食藥署簡任技正陳映樺表示,杏輝的藥物出問題原因包括賦形劑的處方設計不好、包裝藥品的密合度不好和品管流程問題等,也提出預防改正措施報告書,而世達藥品也因多款藥品產品製程異常未經調查即重新加工,然世達未進行根本原因調查也無留有相關紀錄,且生產與管制作業紀錄不實等問題,被要求著衣錠劑(含錠劑、顆粒)產品應停止生產。食藥署7月稽查時也發現,博謙生技公司的原料藥無菌模擬充填試驗結果造假;陳映樺指出,這家藥廠做無菌的原料藥,要定期去驗證操作時的無菌性,但食藥署稽查發現有一些並非無菌,因此發現造假。食藥署表示,依照藥事法規定,會裁處嚴重違反GMP藥廠3萬元到2百萬元,而嚴重違反GMP的藥廠在改進後,食藥署仍會無預警進行複查。

GMP2藥廠7款藥出包 食藥署下令回收違者最高罰500萬
食藥署昨公布GMP藥廠7款藥品下架回收,其中6款為世達藥品工業股份有限公司的藥品,包含咳嗽藥、降血壓藥等,因安定性試驗沒通過,藥效恐不足而回收,另1款則是大豐製藥股份有限公司的季節性過敏鼻炎用藥,因藥效成分釋放太慢而回收。食藥署表示,7款藥品都需在11月初以前內完成回收,否則可處20到500萬元的罰鍰。下架回收的藥品包括「”大豐"抒敏膜衣錠180毫克」、「三化散 Tri-Zyme Powder “S.D.”」、「”世達"三化錠 Tri-Zyme Tablets “S.D.”」、「”世達"咳必定錠 COUGH-PIDINE TABLETS “S.D.”」、「”世達"舒脈寧錠 5毫克」、「達肝膠囊 TALCAN CAPSULES “S.D.”」及「適腸錠 LI SHIH TABLETS “S.D.”」。除了「”大豐"抒敏膜衣錠180毫克」只回收批號9253201的藥品外,其餘6款藥都是全批號回收。食藥署品質監督管理組簡任技正陳映樺表示,食藥署曾在6月底前往世達藥品工業股份有限公司進行查廠,發現該藥廠的檢驗數據有疑慮,因此停止了口服錠劑、顆粒劑型藥品的生產線,並要求藥廠調查。調查結果發現,2款處方用藥、4款指示用藥安定性試驗未通過,意即藥品保存久了主成份恐不足,進而影響藥效,因此必須下架回收。6款藥品適應症分別為幫助消化、鎮咳、高血壓及心絞痛、肝病、腹瀉等。另一方面,處方藥「”大豐"抒敏膜衣錠180毫克」則是因為溶離度試驗不符規格,意即藥效成分在服用後釋放太慢,因此被要求下架回收。陳映樺表示,此次回收的7款藥品,數量都仍待統計,這些藥品都有替代用藥,民眾不至於無藥可用,所有藥品都必須在11月初以前完成回收。若未如期回收,可依《藥事法》處以20-500萬的罰鍰。

鉛中毒凸顯中藥檢驗安全問題 百年莊松榮藥廠GMP認證把關
近日來因鉛中毒事件,讓不少民眾擔心,甚至不敢服用科學中藥,凸顯對科學中藥的認知不足;國內的科學中藥均由GMP中藥廠製造,它的品質是有保障的,所使用之中藥材的重金屬管制必須符合衛福部公告的中藥材含重金屬限量基準,並且中藥廠的GMP必須接受中醫藥司的監督管理,所有市售科學中藥必須符合重金屬限量管制要求 (鉛不得超過5ppm丶鎘不得超過0.5ppm丶砷不得超過3ppm丶汞不得超過0.5ppm),因此消費者可以安心使用中藥廠生產的藥品。台灣首家取得GMP認證的莊松榮製藥廠,自設實驗室檢測中藥材源頭國內超過百年歷史,科學中藥的模範生莊松榮製藥廠,除了是國內第一家取得國內GMP認證的中藥廠(GMP為優良製造標準認證),為了符合從中藥原料的源頭就必須控管,以確保藥品安全無虞,從藥材原料的契作、藥材的存放管理,到藥材製作過程的檢驗,都嚴格把關,更自設高規格檢驗實驗室,以分析毒性與重金屬標準,如此嚴謹標準取得國內科學中藥(即濃縮製劑)六百多張執照,以販售處方藥為主,也就是多人到中醫診所拿到的合格中藥,很多就是出自莊松榮製藥廠。著名莊松榮製藥廠好評的龜鹿二仙膏與加味健步虎潛丸(去虎骨)目前莊松榮製藥廠除了嚴守中藥材原料源頭把關外,更令人記憶深刻的是「龜鹿二仙膏」與「健步虎潛丸」,近期依照衛福部中藥送審提出廣告核定,在各大電視台均能看到產品的蹤影,根據經銷商表示:「龜鹿二仙膏」與「健步虎潛丸」目前詢問量大,不少民眾都有類似的困擾,而從中藥材源頭就把關,並通過GMP認證的百年莊松榮製藥廠出品的中藥產品,也能讓民眾安心服用。莊松榮製藥廠-龜鹿二仙膏 諮詢電話:0800-899-022莊松榮製藥廠-健步虎潛丸 諮詢電話:0800-611-599