美國食品藥物...
」 美國 FDA 美國食品藥物管理局 醫師 新藥
微波爐加熱「不是放中間」!藥師曝正確位置揭原理:不會致癌
微波爐已成為家庭常見家電,不少民眾加熱食物時習慣將餐點置於正中央,不過藥師何峻宇近日於影片中指出,若為一般家中常見的轉盤式微波爐,食物位置應放在邊緣才能提升加熱效率,引發許多網友討論。何峻宇在YouTube影片中先澄清微波爐相關疑慮。他表示,微波爐透過電磁波使食物中的水分子振動並產生熱能,此原理屬於「非游離型輻射」,不會對人體造成致癌風險。他進一步提到,相較於煎、炸等高溫料理方式,微波加熱能降低營養素流失,甚至有機會比水煮更能保留食材原味。何峻宇說明微波爐不會致癌。(圖/翻攝YouTube/三寶藥師)影片中最受關注的則是「加熱位置」。他說明,轉盤式微波爐的微波通常從側邊發射,將餐點放在盤面邊緣,隨轉動即可使食物不同部位接收到較均勻的能量,達到較佳加熱效果;若使用超商常見的平台式微波爐,因為微波從底部釋放,將食物放在中央才是正確作法。此內容曝光後,網路上出現兩種反應。部分網友表示恍然大悟,「難怪中間常常冰冰的」、「原來我誤會它這麼多年」;另一部分網友則提到實際操作不易,「盤子太大放邊邊會卡住轉不動啊」、「放邊緣感覺轉一轉會飛出去,強迫症只能放中間」。此外,粉絲專頁「約翰家庭百貨」也曾分享相同觀點,建議轉盤式微波爐的食物放於邊緣位置,使其在旋轉過程中更均勻受熱;至於無轉盤的機型,由於微波從底部釋放,加熱分布較為一致,可在加熱中段暫停一次,翻動或攪拌內容物,以提升整體受熱效果。針對微波爐是否會造成輻射疑慮,國健署先前則在公告中指出,微波爐是利用電磁波穿透絕緣體,讓食物中的水分子吸收能量後產生加熱效果,並非經由X射線或伽馬射線加熱,因此不會造成食物具有放射性。國健署也引用「美國癌症協會(ACS)」資料說明微波不會改變食物的化學性質,並引用「美國食品藥物管理局(FDA)」資訊補充,微波加熱過程反而可能保留更多維生素與礦物質。

中國生物製藥全面挑戰美國主導地位!北京與上海恐成世界創新中心
中國生物製藥產業正站上關鍵轉折點。隨著研發實力與產業結構的成熟,這個全球第2大製藥市場已被視為進入「創新2.0」階段,從過往追求速度與規模的高速擴張,轉向以品質、價值與商業化能力為核心的發展模式。在部分關鍵領域,中國不僅已追上美國,甚至開始展現超車之勢。據《南華早報》報導,分析公司科睿唯安(Clarivate)於12月8日發布的報告指出,中國生物製藥產業正在經歷1場根本性的優先順序轉換,從資本驅動轉向價值導向,從追逐市場熱點轉向建立可持續競爭優勢。科睿唯安生命科學與醫療健康(Clarivate Life Sciences and Healthcare)資深顧問Alice Zeng指出,過去10年間,中國企業專注於如何進行研發,如今則必須正面迎接藥物上市後的現實問題,包括市場策略、定價能力與重磅藥物的打造。這種轉變發生之際,美國對中國生技能力的警戒也持續升高。美國國會多年來推動的《生物安全法案》(Biosecure Act),已於12月18日隨國防法案正式立法,授權行政部門限制與特定中國生物科技公司的聯邦合約往來。儘管法案未直接點名企業,但其長期影響,特別是在早期藥物研發與合作層面,仍被業界高度關注。然而,限制措施能否有效遏止中國的生物製藥崛起,正逐漸受到質疑。今年4月,美國兩黨立法委員會「新興生物科技國家安全委員會」(National Security Commission on Emerging Biotechnology)警告,美國僅剩3年時間維持或重奪生物科技領導地位,並於12月直言,美中差距縮小的速度「快於預期」。該委員會形容,1個以北京與上海取代舊金山與波士頓、成為全球生物製藥創新核心的世界,已不再只是想像。在實務層面,中國企業已在PD-1癌症藥物等領域展現競爭力。由上海君實生物(Shanghai Junshi Biosciences)研發的特瑞普利單抗(Toripalimab),於2023年獲美國食品藥物管理局(Food and Drug Administration,FDA)核准治療鼻咽癌,成為首款獲准對抗此類侵襲性癌症的藥物。即便在美國的售價遠高於中國,該藥仍比美國同類產品便宜約2成,突顯中國在成本與供應鏈上的優勢。數據同樣反映這股趨勢。2004年至2023年間,全球共推出942種新型活性物質,其中美國居首、中國緊隨其後。根據科睿唯安統計,中國已成為全球新分子實體(New molecular entity,NME)首次上市數量排名第2的國家,並在2024年占比達18%。在標靶蛋白質降解(targeted protein degradation,TPD)等前沿技術上,中國於論文發表、專利與研發管線的全球占比均居領先地位。支撐這一躍進的,還包括龐大的科研產出與政策配套。2024年,中國發表的生命科學論文占全球近3成,幾乎是9年前的2倍。官方推出的30天臨床試驗快速審批通道,以及串聯研發、融資、監管與健保的政策體系,進一步壓縮藥物上市時程,使中國的審批速度已與美國幾乎同步。這樣的環境,也吸引國際藥廠重新思考市場布局。越來越多企業選擇優先向中國國家藥品監督管理局(National Medical Products Administration,NMPA)申請上市,再進軍其他成熟市場。對於面臨激烈競爭與高成本壓力的企業而言,中國不僅是龐大的銷售市場,更可能成為全球化布局的起點。然而,低成本亦帶來結構性挑戰。Alice Zeng指出,中國來源藥物的價格優勢,正使印度、南韓等新興市場的競爭變得更加激烈,甚至可能壓縮全球創新生態的利潤空間。她警告,若創新藥物只能以最低價競爭,將難以支撐長期研發投資,反而削弱整體產業的可持續性。即便如此,多數觀察者認為,要在創新藥物研發上全面複製中國的生態系並不容易。從基礎研究到供應鏈整合,再到臨床試驗與市場規模,中國已形成高度完整的體系。正如美國新興生物科技國家安全委員會所言,中國在生物製藥創新上超越美國的世界,已不再是未來假設,而是1個正在成形的現實。

藥華藥再捷報!Ropeg完成申請美國ET藥證 拚2026取證
藥華藥(6446)再報佳績,11月營收再創新高之外,旗下新藥Ropeginterferon alfa-2b-njft(Ropeg,即P1101)於美國申請原發性血小板過多症(ET)新適應症藥證進展順利,已完成與美國食品藥物管理局(FDA)的送件說明會議(AOM),預計2026年取證。藥華藥於12月8日以視訊方式與FDA審查官員召開ET藥證申請之AOM,AOM(Application Orientation Meeting)為公司提交藥證申請後,與FDA審查官員團隊舉行的首次正式會議。會中,公司向FDA審查官員深入說明申請文件架構、臨床效益摘要、藥物機轉及安全性等重點。透過AOM,公司得以引導審查官員在龐大的臨床資料中聚焦關鍵數據,並協助FDA在啟動實質審查前即可掌握送件資料的核心脈絡。藥華藥11月營收15.5億元,月增10.63%,年增53.02%,已連續三個月刷新單月歷史新高。藥華藥2025年10月底向美國FDA申請Ropeg的ET藥證,並已獲FDA確認,若於收件日起60日內FDA未通知其他意見,本案將依法於2025年12月29日正式進入實質性審查程序。 Ropeg為藥華藥自行發明生產的新一代創新長效型干擾素,至今已獲全球約50個國家核准用於真性紅血球增多症(PV)患者並上市銷售,包括歐盟、美國及日本等主要新藥市場,全球用藥人數及銷售穩健成長。持續拓展Ropeg新適應症,ET與PV同屬骨髓增生性腫瘤(MPN),病人數亦相近。

疑未標示小麥恐致過敏!哈根達斯召回黑巧克力冰淇淋棒
美國知名冰淇淋品牌哈根達斯(Häagen-Dazs)近日因潛在過敏風險,宣布召回部分批次的黑巧克力迷你冰淇淋棒。生產商醉爾斯冰淇淋公司(Dreyer’s Grand Ice Cream, Inc.)指出,這些產品可能含有未標示的小麥成分,對小麥過敏或高度敏感者可能造成嚴重甚至危及生命的反應。據美國美國食品藥物管理局(U.S. Food and Drug Administration,FDA)公告,受影響產品為「哈根達斯黑巧克力迷你冰淇淋棒」(Häagen-Dazs Dark Chocolate Mini Bars),6入裝,批號為LLA519501,有效期限至2027年1月31日。醉爾斯公司追蹤後發現,該批產品曾於多州的克羅格(Kroger)及巨鷹超市(Giant Eagle)銷售。克羅格門市涵蓋全美29州,包括加州、德州、伊利諾、俄亥俄與華盛頓等;巨鷹則分布於印第安納、馬里蘭、俄亥俄、賓夕法尼亞及西維吉尼亞五州。公司與FDA合作進行召回,並強調其他哈根達斯產品或批次並未受到影響。醉爾斯在聲明中表示,問題可能出現在生產初期,「含小麥的原料被誤封入錯誤包裝」,導致標籤上未顯示小麥成分。該公司正持續進行內部調查,以釐清製程問題。截至11月4日,尚未接獲任何疾病或過敏反應通報。醉爾斯強調:「產品的安全、品質與完整性是我們的首要任務,對於造成的不便,我們深表歉意。」當局呼籲所有對小麥過敏或敏感的消費者切勿食用此產品,應立即丟棄,或退回原購買商店以獲全額退款。

大陸製藥實力匹敵歐美? 美媒:成貿易戰武器
美陸達成1年休戰協議後,雙方貿易角力並未止歇。美媒指出,在稀土與農業外,北京手中仍握有一項「尚未使用的武器」,也就是全球藥品供應鏈,因為大陸製藥實力現已匹敵歐美。專家警告,若陸美再陷對立,北京可藉切斷藥品與原料出口施壓,而美國已「完全喪失獨立生產抗生素的能力」,對陸依賴已構成潛在風險。文中稱,大陸製藥業在政府輔助下已完成產業升級,研發水準足以匹敵歐美,從基本的抗生素到先進製劑,皆具備相當競爭力。哥倫比亞大學學者費希曼指出,開放式貿易體系「並非為當前的地緣政治競爭而設」,卻正讓大陸得以引進外國技術逐步取代西方製造商。反觀美國,有專家警告美國已「完全喪失獨立生產抗生素的能力」。《中國處方》作者吉布森直言,由於大量生產環節轉移到海外,美國製藥整體產能已大幅流失。此外,美國食品藥物管理局(FDA)在國內進行突擊檢查,但在大陸需事先通知,且簽證程序繁瑣,讓大陸藥廠可提前準備、規避稽查。美國參院老齡問題特別委員會指出,美國藥品自製比例自2002年的83%降至2024年的37%。同時,30%的藥品活性成分完全依賴大陸供應;若計入印度生產、但使用大陸原料的藥物,比例更高達60%。美國外交關係委員會研究員黃嚴忠表示,美國製藥要恢復完整供應鏈「幾乎不可能」。大陸已建立大型產業園區,能以低運輸成本提供一站式原料採購與中間體生產,形塑難以撼動的優勢。分析認為,若西方要在此領域與大陸抗衡,必須推動「生產導向」的合作戰略。日本已開始資助國內企業重啟藥物原料生產,並尋求產品能免稅輸入美國。若能形成「美日歐」供應聯盟,或可避免歐洲最後一家抗生素工廠外移大陸的慘劇重演。
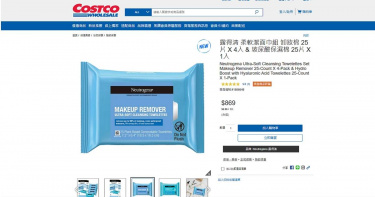
露得清卸妝濕巾疑遭細菌污染 在美召回1.5萬包產品
美國食品藥物管理局(FDA)近日宣布,知名護膚用品大廠露得清(Neutrogena)旗下「超柔卸妝濕巾」(Neutrogena Makeup Remover Ultra-Soft Cleansing Towelettes),發生「格氏多元桿菌」(Pluralibacter gergoviae)污染事件,已經在美國展開召回。綜合外媒報導,美國食品藥物管理局近日發布公告指出,露得清母公司「Kenvue」在對部分產品進行格氏多元桿菌檢驗時,結果呈現陽性反應。這種細菌對添加在化妝品裡的抗菌劑「對羥基苯甲酸酯」具有抗藥性。FDA指出,格氏多元桿菌對一般民眾威脅不大,但對免疫力低下或慢性病患者,可能導致眼部、泌尿道感染或是呼吸道疾病,甚至引發敗血症。事件曝光後,母公司「Kenvue」已依照FDA的指示對美國境內展開產品召回。據了解,被召回的產品批號為「1835U6325A」,被銷售到德州、南卡羅萊納州、喬治亞州和佛州。目前,產品污染來源尚未確定,也並未傳出有相關病例通報,不過Kenvue發言人指出:「消費者健康與安全是我們的首要考量,儘管產品符合出廠規格,但基於謹慎原則主動召回。」發言人同時強調,其他露得清產品均未受到影響。據了解,這款卸妝濕巾在台灣好市多也有販售,不過除產品批號「1835U6325A」以外均非召回對象。

超商贈「牛奶嘴蓋」引食安疑慮 專家見材質示警:強調為一次性使用
近期全家超商推出滿額贈活動,消費者購買指定品牌鮮奶可獲贈一款仿乳牛乳頭造型的「牛奶嘴蓋」,外型吸睛宛如現擠牛奶,迅速在網路上引發討論。然而,該贈品為3D列印製作,引起食品安全專家關注,憂心其材質與製程恐對健康構成風險。據了解,該款牛奶嘴蓋為一次性塑膠商品,材質為PETG(聚對苯二甲酸乙二醇酯與環己二醇共聚物),包裝上明確標示不可微波、不可盛裝熱飲,建議使用冷水清洗,且不得使用漂白劑或含氯清潔劑。但部分消費者可能忽略其「僅供一次使用」的警示。國立台灣海洋大學安全與風險管理研究所教授林詠凱在臉書上表示,透過儀器分析可見,該產品表面具有明顯層紋,判斷為3D列印製成。他指出,由於牛奶屬高營養液體,若盛裝於表面粗糙的容器中,易形成生物膜與微生物孳生溫床,即使經多次清洗,仍難以完全避免塑膠添加劑或微粒遷移至乳品中。林詠凱進一步呼籲,主管機關應針對以3D列印製成的食品接觸器具,從材料選擇、列印流程到消費端教育,制定完整規範。此外,他提醒,大多數3D列印機所使用的噴頭為鉛或銅合金材質,若未經食品級處理,潛藏重金屬遷移風險,不可輕忽。除了專家意見,該產品也在3D列印社群中掀起熱烈討論。有網友指出,列印用的線材常加入各式添加劑以改善加工性能,實際成分可能已與標示不同。且線材多數未經食品級檢測,在製程與成本考量下,部分業者並不會主動送驗,安全性令人擔憂。對此,食品藥物管理署食品組簡任視察林蘭砡表示,美國食品藥物管理局已核准PETG作為食品接觸材質,食藥署立場是只要符合我國食品器具容器衛生標準,即可使用。然而,她亦提醒,使用3D列印製作食品器具時,應遵守《食品良好衛生規範準則》,特別是線材儲存與列印設備接觸部位應避免汙染。林蘭砡補充,若3D列印成品表面有層紋或不平整,容易造成清潔不完全,進而引發安全疑慮。建議消費者避免重複使用一次性塑膠製品;若業者希望提供可重複使用版本,應採表面塗層處理並加註清晰使用說明。

WHO警告:印度3款止咳糖漿受污染!釀21名孩童死亡
世界衛生組織(World Health Organization,WHO)於美東時間13日發布健康警示,提醒全球關注在印度發現的3款受污染止咳糖漿,並敦促各國當局若發現這些藥品應立即向WHO通報。據《路透社》報導,WHO指出,受影響的止咳糖漿包括Sresan Pharmaceutical的「Coldrif」、Rednex Pharmaceuticals的「Respifresh TR」,以及Shape Pharma的「ReLife」特定批次。WHO表示,這些受污染的藥品具有重大風險,可能導致嚴重甚至危及生命的疾病。印度藥品監管機構「中央藥品標準控制組織」(Central Drugs Standard Control Organization,CDSCO)告知WHO,這些糖漿曾被印度中央邦(Madhya Pradesh)欽德瓦拉市(Chhindwara)年齡不滿5歲的21名兒童服用,而這些孩子近期已不幸身亡。經檢測,該止咳藥中含有有毒的有機化合物「二甘醇」(diethylene glycol),含量幾乎是允許上限的500倍。CDSCO表示,這些受污染藥品尚未出口印度,也沒有非法出口的證據。此前,美國食品藥物管理局(U.S. Food and Drug Administration,FDA)也於10日確認,這些含毒止咳糖漿並未運往美國。

廚房用具恐釀癌症、自閉症 美FDA示警:化學物質滲入食物
美國食品藥物管理局(FDA)近日發布緊急警告,指出市面上部分廚房用品可能會釋出含鉛等有毒金屬,滲入食物中,長期接觸恐與癌症、自閉症等健康問題有關。根據英媒《每日郵報》(Daily Mail)報導,FDA調查指出,美國零售通路販售的多款鍋具產品,在檢驗中發現含有「鉛」,此為對人體有害的重金屬,恐使食物遭到污染,不宜繼續使用。遭點名的四項產品全數來自印度,品牌分別為「Tiger White」、「Silver Horse」及「JK Vallabhdas」,材質皆為鋁製,產品包括三款平底鍋及一款牛奶鍋。這些產品是在紐約與伊利諾州的三間零售通路中被發現,包括「Mannan Supermarket」、「Patel Brothers」及「Indiacos」等超市。不過目前尚不清楚這些商品,是否也流通至其他地區。FDA呼籲消費者儘速檢查家中,是否有上述品牌的鍋具,若發現產品可能含鉛,應立即停用並丟棄。廚具販售業者與進口商也被建議主動聯繫FDA,確認產品是否符合安全與法規標準。FDA指出,某些進口鋁製、鋁合金與黃銅廚具可能使用回收材料(如汽車零件)製成,製程中若未妥善處理,將可能導致鉛等重金屬污染。報導指出,醫學研究顯示,鉛中毒與神經系統疾病、學習障礙、自閉症、腎臟病、心血管疾病、出生缺陷甚至癌症有關,且鉛會在體內器官累積,造成長期傷害。FDA強調:「即使是極低劑量的鉛,也可能對健康造成嚴重影響。」兒童與胎兒因體型較小、新陳代謝快速,對鉛的敏感度更高,若長期攝取含鉛食物,即使無明顯症狀,也可能出現智力下降、行為異常等發展遲緩問題。鉛中毒症狀包括腹痛、嘔吐、嗜睡、易怒、虛弱、情緒改變,甚至癲癇發作與昏迷。而成人若接觸鉛,也可能出現高血壓、腎功能受損、不孕症、癌症風險上升與神經系統退化等問題。事實上,目前FDA已全面禁止含鉛成分用於食品接觸產品,包括鍋具、餐具等。此外,華盛頓州也將於2026年1月1日起,率全美之先禁止製造及販售含鉛超過5ppm的金屬廚具,範圍包括鍋柄、把手等所有接觸部件。

高壓氧艙突爆炸!5歲弟被困燒成焦屍 媽目睹「烈焰吞噬兒」崩潰
美國密西根州發生一起駭人聽聞的醫療悲劇。一名年僅5歲男童今年初在高壓氧艙治療過程中,因爆炸起火被困艙內當場喪命。家屬日前向法院提起高達1億美元的求償訴訟,控訴醫療機構及製造商「為了牟利而漠視人命」。NBC報導,罹難男童名叫湯瑪斯・庫珀(Thomas Cooper),來自密西根州皇家橡樹市。庫珀父母指出,位於底特律郊區特洛伊的「牛津中心」(Oxford Center)多次建議他接受高壓氧治療,用於改善睡眠呼吸中止症及注意力不足過動症,但他們從未被告知艙體存在致命風險。悲劇發生在今年1月31日,湯瑪斯在艙內治療時突發大火。母親第一時間衝上前試圖救人,被烈焰灼傷手臂,仍無法阻止愛子在眼前被大火吞噬。律師哈靈頓(James Harrington)表示,相關業者不僅沒有警告,反而積極鼓勵湯瑪斯進入艙內,目的只是為了賺錢,「被告明知艙內一旦發生火災,病人根本無法存活,卻仍執意營運。」家屬訴訟將8方列為被告,包括牛津中心、執行長與3名員工、關聯基金會、物業業主,以及氧艙製造商Sechrist Industries。訴狀指出,「這起死亡不是意外,而是被告冷酷無情、企業貪婪的必然結果。」目前,牛津中心部分員工除面臨民事求償,也遭到刑事起訴。創辦人彼得森(Tamela Peterson)、安全經理莫斯特勒(Jeffrey Mosteller)、管理助理馬肯(Gary Marken)各被控二級謀殺與過失殺人;當時操作艙體的員工莫菲特(AletaMoffitt),則被控過失殺人及竄改醫療紀錄。目前4人均不認罪。檢方指出,火災肇因於靜電引燃,而中心人員未遵守基本安全規範。專家強調,高壓氧艙提供100%純氧,雖可協助治療部分傷病,但環境高度易燃,稍有疏失就會釀災。報導指出,美國食品藥物管理局(FDA)僅核准高壓氧治療用於13項病症,包括一氧化碳中毒、糖尿病足傷口及潛水夫病;但牛津中心宣稱可治療超過百種疾病,甚至涵蓋自閉症、失智症與癌症,相關療效並未獲FDA認可。湯瑪斯的不幸死亡,也凸顯美國養生產業對高壓氧艙的濫用。FDA已提醒,部分療效說法「缺乏證據」,呼籲患者應選擇通過專業醫學會認證的機構。然而,牛津中心並不在名單內。律師沉痛表示,湯瑪斯的父母無論走到哪裡都會想起兒子,「孩子被困艙內,眼睜睜看著母親卻無法獲救,這是最殘酷的離別方式。」
美國CDC「不再建議成人接種新冠疫苗」?疾管署緊急發聲了
今天(20日)有報導稱美國疾病管制中心(CDC)預防接種諮詢委員會(ACIP)不再建議成年人接種新冠疫苗。對此,我國疾管署特別澄清,相關報導內容與美國官方發布之新聞稿內容有所出入,事實上ACIP仍建議成人應於評估感染後併發重症之風險接受新冠疫苗接種,而非不再建議成年人接種。疾管署指出,美國CDC所屬預防接種諮詢委員會19日最新公布2025-2026年新冠疫苗接種建議,對於成人高風險對象仍建議接種新冠疫苗,僅是新增共同臨床決策,即民眾與醫護人員討論依風險評估決策接種,而非不建議接種。疾管署表示,美國ACIP雖建議增加「共同決策」,美國多州政府與相關醫學會(包含美國兒科醫學會、美國婦產科醫學會、美國傳染病學會及美國家庭醫學會)仍維持積極立場,建議幼童、孕婦及成人高風險對象等接種新冠疫苗,是防範重症與死亡的重要措施。疾管署說明,我國衛生福利部傳染病防治諮詢會預防接種組(ACIP)於今年6月12日會議,係經參酌世界衛生組織(WHO)針對不同年齡層與風險族群接種建議、美國食品藥物管理局(FDA)於期刊發表建議從普遍接種轉為風險導向,以及美國CDC、英國、德國、法國及日本等多數國家建議以長者、高風險對象、機構住民及醫事工作者等為主要接種對象,同時考量國內接種情形、疾病傳播風險、幼兒抵抗力較弱且仍有重症個案發生等因素,建議今年秋冬新冠疫苗接種對象調整為10類對象。疾管署呼籲,為防範秋冬可能疫情,預計自今年10月1日起如期推動「左流右新」,新冠疫苗仍如期與流感疫苗同步分2階段開打,其中除50-64歲無高風險成人於第2階段(今年11月1日起)開打,其餘新冠疫苗之9類公費接種對象皆於第1階段開打,以促進共同接種,提升接種率,有效降低重症及死亡發生風險。

Neuralink宣布全球12名患者植入腦機介面晶片 使用時間逾2千天
美國科技巨擘馬斯克(Elon Musk)旗下醫療植入公司Neuralink週二宣布,目前全球已有12名患者使用其腦機介面晶片(Brain Computer Interfaces, BCI),累計使用時間超過1萬5,335小時(約2,000天),在腦部植入技術發展上邁出關鍵一步。路透社報導,Neuralink近日成為焦點。首位接受植入的患者阿巴(Noland Arbaugh)接受《財富雜誌》(Fortune)專訪時透露,他在2016年因游泳意外導致下半身癱瘓,植入晶片後開始重新接觸電玩與語言學習,並形容自己正「努力追趕過去8年的空白」。Neuralink表示,這些患者的累積使用紀錄顯示裝置穩定運作。公司同時於8月27日與9月8日在加拿大多倫多大學健康網絡醫院(UHN),首度於美國境外進行植入手術,作為為期4年的臨床試驗一部分,研究目標是讓四肢癱瘓患者能透過意念操控電子設備。此外,Neuralink今年7月也獲得英國監管機構核准,將啟動GB-PRIME臨床研究,同樣聚焦癱瘓患者如何藉由腦機介面與數位世界互動。馬斯克在2020年曾表示,期望最終將腦晶片與植入手術成本壓低至「僅需數千美元」。自2023 年獲得美國食品藥物管理局(FDA)核准開展人體試驗以來,Neuralink已逐步拓展至國際舞台,並朝著讓腦機介面成為可負擔醫療方案的願景邁進。

二、三手菸也傷毛小孩!罹癌風險飆2至4倍 存活1年機率不到1成
調查顯示,約每3名成人就有1人受家庭二手菸影響,近3成青少年未能倖免,甚至貓狗等毛小孩都可能因二手菸罹患呼吸道疾病及癌症。國民健康署呼籲打造無菸家庭,鼓勵民眾善用免費戒菸服務,避免心愛的家人與毛小孩暴露於二手、三手菸害之中。根據113年國人吸菸行為調查結果顯示,18歲以上人口家庭二手菸暴露率為35.6%,平均3個人就有1人暴露於家庭二手菸;另112年青少年吸菸行為調查發現,國中生及高中職生家庭二手菸暴露率分別為25.9%及26.0%,顯示近3成青少年仍被迫生活在二手菸環境中。時值暑假,學生居家時間長,國民健康署署長沈靜芬呼籲家長,共同建立無菸健康環境,為家人勇敢戒菸。沈靜芬指出,根據研究顯示吸菸是多種傳染性疾病的危險因素、損害上呼吸道、抑制肺部免疫功能,並可能導致患者疾病程度惡化,且吸菸者出現COVID-19嚴重症狀的可能性較非吸菸者高1.4倍,入住加護病房、使用呼吸器或死亡可能性較非吸菸者高2.4倍。臺灣兒科醫學會前理事長李宏昌醫師說明,同住家人若有吸菸習慣,對其他家人健康有嚴重影響,即使未吸菸也可能因二手菸、三手菸而增加罹患肺癌等疾病的風險。研究顯示若妻子為非吸菸者,先生每日吸菸超過20根,妻子罹患肺癌的危險性是非暴露二、三手菸者的3.4倍;而若和先生結婚超過30年,妻子罹患肺癌的危險性是非暴露二、三手菸者的3.1倍,且吸菸是主要危險因素,佔所有肺癌診斷病例的80%至90%,值得注意的是,吸菸導致肺癌的危險性是非吸菸者的15至30倍,雖然目前肺癌第1期的5年存活率有將近9成,但肺癌第4期存活率僅1成,民眾萬不可忽視吸菸的危害。柚子小兒科診所院長陳木榮表示,很多癮君子以為在陽臺或家門口就不會影響家人,然而美國疾病管制與預防中心(CDC)指出,二手菸可以透過門口、牆壁裂縫、電線、通風系統和管道傳入,且即使短暫接觸也會使血小板變得更黏稠、損害血管內壁,增加心臟病發作的風險,若暴露於二手菸環境60分鐘內,會產生發炎現象、影響呼吸功能,且影響至少持續3小時,並可能導致嬰兒猝死症候群(SIDS)、兒童呼吸道感染、耳部感染和氣喘發作。中華民國獸醫師公會全國聯合會理事長譚大倫透露,根據美國食品藥物管理局資料顯示,當寵物直接吸入二手菸,或透過皮膚、舔主人的頭髮、皮膚和衣服接觸到菸草化合物(三手菸)時,都會直接對毛小孩造成危害,長期暴露於二手菸、三手菸環境下,可能會引發過敏反應、呼吸系統疾病或罹患鼻癌和肺癌;而當貓咪梳理毛髮時,易吸入落在毛髮上的三手菸,導致口腔癌的發生,其罹癌機率相較無菸害環境下高出2至4倍,且貓咪罹口腔癌後,即使接受過化療、手術或放射治療,其確診後存活1年機率不到1成。國民健康署提醒民眾,為了最愛的毛小孩,及早戒菸,以防憾事發生。

臺灣每3名學童1人過重!兒科醫示警:恐延續至成年 6項實用建議曝
根據衛生福利部國民健康署統計,臺灣約每3名學童就有1人有過重或肥胖的情形。高熱量飲食、運動量不足,以及長時間使用電子產品,是導致兒童肥胖率逐年上升的主因。新竹臺大分院小兒部林函怡醫師表示,「小時候胖不是胖」的觀念早已過時。兒童期的肥胖不僅影響眼前健康,更可能延續至成年,增加罹患糖尿病、心血管疾病與代謝症候群等慢性病的風險。林函怡醫師進一步說明,肥胖會提升胰島素阻抗,導致第二型糖尿病風險升高;脂肪若過度堆積,還可能造成非酒精性脂肪肝,嚴重時甚至演變為肝纖維化或肝硬化。此外,肥胖也會對心理造成影響,部分兒童可能因身形焦慮、自尊心低落而出現憂鬱傾向,進而影響社交能力與學習表現。面對兒童肥胖問題,醫師指出,改善生活型態是控制體重的第一步,也是最關鍵的一步。她提出6項實用建議,協助家長與孩子一起打造健康生活:1、飲食:多攝取蔬果、全穀類等原型食物,減少甜點、零食與油炸品攝取。2、以白開水取代含糖飲料:避免習慣性攝取高糖飲品。3、全家共餐、細嚼慢嚥:放慢用餐速度,鼓勵與家人共餐,讓孩子從家庭中培養良好飲食行為。4、每天規律運動:依世界衛生組織建議,兒童與青少年每天應進行至少60分鐘中高強度活動,如快走、跳繩、球類運動等,有助促進心肺功能與骨骼健康。5、限制3C使用時間:每日建議不超過2小時,避免久坐影響代謝。6、充足睡眠:睡眠不足會增加肥胖風險,建立規律作息、確保良好睡眠品質,是維持體重的關鍵。林函怡提到,近年國際間針對青少年肥胖的藥物治療已有新進展。2022年,美國食品藥物管理局(FDA)核准GLP-1類藥物「Semaglutide(司美格魯肽)」應用於12歲以上、符合診斷標準的青少年。該藥原用於治療第二型糖尿病,具有延緩胃排空、提升飽足感與抑制食慾等作用。臨床研究顯示,連續使用68週後,青少年BMI平均下降逾16%。醫師強調,「藥物治療僅為輔助工具,使用期間可能伴隨噁心、嘔吐等副作用,仍須在專業醫療團隊評估下進行,並應建立在良好的飲食與運動基礎上,才能真正發揮效果。」肥胖帶來的不僅是外型改變,更影響孩子的長期健康與心理發展。新竹臺大分院提醒家長,應及早關注孩子的生活習慣與身體變化,從飲食、運動與睡眠3方面著手,幫助孩子在健康中成長,在自信中茁壯。

營養系畢業生聽信AI建議 改用溴化鈉煮飯陷幻覺偏執「強制送精神監護」
美國一名60歲男子,因聽信ChatGPT的飲食替代建議,用溴化鈉取代食鹽長達三個月,最終因嚴重溴中毒住院三週,還出現幻覺與偏執等精神病症狀。該男子曾主修營養學,但沒有精神疾病或重大醫療病史。根據《美國內科醫師學會期刊》與《Ars Technica》報導,該名男子在閱讀到過量攝取食鹽(氯化鈉)可能危害健康的資訊後,決定自我實驗,將飲食中所有氯化物剔除。在與ChatGPT互動後,該名男子認為,可以用溴化鈉替代氯化鈉,便在網路購買溴化鈉,並連續三個月將其作為日常烹調用鹽。三個月後,男子被送往急診室,聲稱鄰居企圖毒害他,拒絕飲用醫院提供的水,並透露自己平時在家蒸餾飲用水且採取極端素食。檢查發現,他缺乏多種微量營養素與維生素,血液中的溴化物濃度更高達每公升1,700毫克,遠超正常的每公升0.9至7.3毫克。醫療團隊診斷為溴中毒,這種情況在20世紀初期並不罕見,當時溴化物廣泛用於鎮靜劑與安眠藥,但因容易在體內累積、損害神經功能,美國食品藥物管理局(FDA)自1989年起已全面禁用。入院首日,男子病情迅速惡化,出現聽覺與視覺幻覺、偏執加劇,甚至企圖逃離醫院。醫院隨即對他實施強制精神監護,並注射抗精神病藥物。治療團隊以大量輸液與電解質進行「積極鹽水利尿」,加快排出體內溴化物。經過三週治療,症狀才逐漸緩解。病情穩定後,該名男子向醫師透露,之所以會用溴化鈉替代氯化鈉,除了本身大學營養學背景外,還有自行搜尋資料的影響,當中還包含在ChatGPT的回應中看到「氯化物可由溴化物替代」的說法,但該建議很可能是針對非食用用途,如清潔或泳池消毒。負責撰寫病例的醫師雖未取得實際對話紀錄,但推測男子可能使用的是ChatGPT 3.5或4.0版本,並指出ChatGPT確實會提到溴化物,卻未清楚警告健康風險,也沒有進一步詢問使用情境。OpenAI在使用條款中已明確說明,ChatGPT的內容「可能並非始終準確」,不應作為唯一事實來源或專業建議的替代,更不適用於診斷或治療健康狀況。但該男子未經專業醫療評估就採納建議,最終導致嚴重中毒。醫師也警告,在資訊氾濫的時代,缺乏醫學背景與判斷力,貿然聽從人工智慧的健康建議,可能釀成嚴重後果。

好市多自有品牌牛奶過期7天沒壞 背後原因會員讚爆
美式賣場好市多(Costco)販售商品被認為CP值高,又時常推出優惠,吸引不少民眾前往採買。而好市多自有品牌Kirkland的牛奶是熱賣商品,除了便宜外,保存期限也比其他品牌長,甚至過期7天還不會變質。近日有外媒分析背後原因,主要是好市多牛奶經過比政府標準還嚴格的檢驗,難怪能放比較久。近日有國外的好市多會員在論壇Reddit發文表示,他發現好市多自有品牌Kirkland的牛奶在過期7天也沒有變質,獲得其他會員贊同,在底下補充說,「我比較喜歡好市多的牛奶,因為它真的比其他牌子放更多時間。」根據外媒《Food & Wine》對此分析,Kirkland的牛奶之所以比其他品牌耐放,極大可能與他們的牛奶得經過比政府標準更嚴格的檢驗與品質控管有關。在美國販售的A級鮮奶都需要遵守美國食品藥物管理局(FDA)基本安全規範,像是細菌與細胞數量控制、擠乳後快速降溫等,大多乳品廠一年只會進行1至2次檢測。不過好市多與其他乳品廠不同,依2023年《食品安全與品質稽核準則》顯示,負責生產Kirkland牛奶的供應商每年至少需接受一次突擊檢查(中國地區則為兩次),其中還必須達到「零重大缺失」。若檢測評分低於85%,在60天內還要重新稽核;供應商未配合額外稽核,檢查員也會再次訪查,而費用還是由供應商負擔。除此之外,Kirkland牛奶在出貨前都要接受多達60項微生物測試,凡有1項沒達標就不能出貨。牛奶處理過程中用水的檢測頻率也高於FDA要求,每3年就會更換稽核人員,防止長期合作有疏漏。在好市多層層嚴格把關的措施下,才能讓消費者喝到的每一口牛奶都更安心。許多會員也在得知自己喝到的牛奶經過這麼多關卡,盛讚好市多在這方面品管上有多用心。

數十萬罐Dr.Pepper被美國召回 FDA:可能產生健康問題
美國近日召回數十萬罐Dr.Pepper Zero Sugar汽水,因為Dr.Pepper將其誤標成含糖版本,上月23日首次召回,本月5日再列入第二級召回,因為可能會產生健康問題。據《印度時報》報導,美國食品藥物管理局(FDA)已證實此召回事件,並正式將其列為第二級健康風險(Class II Recall),受影響產品若被喝下肚,可能導致「暫時性或可醫療逆轉的不良健康影響」。據FDA資料,這次召回涉及1.9萬箱的「Dr.Pepper Zero Sugar」12盎司鋁罐裝汽水,分為12罐裝與24罐裝兩種包裝,這些產品已配送至佛羅里達州、喬治亞州與南卡羅來納州等地的零售店。因為罐身標示「Zero Sugar(零糖)」,但實際上是全糖汽水,這對患有糖尿病、肥胖、心臟疾病或正在控制糖分攝取的人而言,可能造成健康風險。據悉,這問題在上月23日由產品製造商Keurig Dr Pepper主動發起召回後才曝光,FDA於6月5日正式列為第二級召回。對此,Keurig Dr Pepper回應,這批汽水是在獲得許可的PepsiCo裝瓶廠生產,相關產品已下架,並未收到任何相關的投訴或疾病報告。一般來說,Dr.Pepper Zero Sugar是用阿斯巴甜(aspartame)製作,提供比含糖汽水更低卡的選擇。對於有血糖問題的人而言,當預期喝的是無糖飲料卻攝取大量糖分,風險可能會升高。

鉅怡智慧AI醫材軟體再獲FDA認證 引領台灣生醫科技走向全球
AI 醫材軟體新創鉅怡智慧(FaceHeart)再捷報,旗下 FaceHeart Vitals SDK 非接觸影像式生理資訊量測軟體於4月9日再度獲得美國食品藥物管理局(FDA)二級醫療器材軟體認證,獲准用於呼吸頻率的量測。繼去年心率量測技術首度取得FDA認證後,這項新的里程碑不僅展現了FaceHeart Vitals在臨床上的有效性與安全性,更進一步拓展其在居家醫療、長期照護及遠距醫療等應用領域的發展潛力。鉅怡智慧進一步表示,FaceHeart Vitals為全球首個通過美國FDA認證的非接觸式生理資訊量測產品,使用者無須配戴任何醫療器材,僅需使用一般手機鏡頭,進行約50秒「臉部掃描」,即可零接觸、連續的量測心率、血壓、血氧、呼吸頻率、心率變異度等生理數值。透過FaceHeart Vitals內AI技術,病患可以使用手機追蹤健康狀況,醫師也能獲取即時健康數據。美國FDA認證 FaceHeart Vitals呼吸量測偏差值為每分鐘±2 次,為其進入國際智慧醫療產業奠定堅實基礎。FaceHeart Vitals產品示意圖。(圖/鉅怡智慧提供)此項產品運用「遠程光電容積脈搏波信號技術」(remote Photoplethysmography, rPPG),能夠透過一般RGB鏡頭偵測臉部細微的顏色變化,並搭配 AI 模型進行分析解讀。FaceHeart Vitals 以軟體開發套件(SDK)的形式,靈活整合於智慧型手機(iOS/Android)、平板電腦、電腦(Windows)、智慧電視、智慧鏡等裝置,將隨手可得的電子設備瞬間轉變為醫療器材。鉅怡智慧創辦人暨國立陽明交通大學講座教授吳炳飛博士表示,「繼 2023 年心率首次通過FDA認證後,此次呼吸頻率的認證充分展現鉅怡智慧的技術領導地位;而FaceHeart Vitals 將在健康照護產業中扮演極為關鍵的角色,我們期待在美國FDA的肯定下,引領台灣自主研發的生醫科技走向全球!」「鉅怡智慧目前已與台大、長庚、榮總等多個國內外醫療中心合作建立臨床影像資料庫,收集超過3億筆影像資料,打造多個AI醫療模型,深化在預防醫學、精準醫療等相關應用。」負責FDA認證及臨床試驗的鉅怡智慧共同創辦人鐘孟良博士表示,「我們今年將推出了心血管功能參數,包含心房顫動(AtrialFibrillation)檢測、心臟衰竭風險、心血管年齡、心血管 BMI等,擴展 rPPG 技術的應用範疇,希望提早篩檢出心房顫動的病患,降低因潛在疾病產生之健康風險。」FaceHeart CardioMirror智慧鏡。(圖/鉅怡智慧提供)鉅怡智慧主要投資夥伴台杉投資生技基金執行合夥人黃立鑫指出,「在全球醫療數位化加速的趨勢下,FaceHeart Vitals具有顯著的市場潛力。其低成本、高普及性的解決方案能有效解決醫療資源短缺的問題,同時也為預防醫學提供關鍵數據支援。」台杉投資生技基金投資協理林世永博士亦指出,「鉅怡智慧再次獲得FDA認證凸顯其堅強的技術實力,隨著在各項認證及應用場景的持續拓展,將為全球醫療生態系帶來革命性的影響。」鉅怡智慧官網:https://www.faceheart.com

剛出生就罹患罕見疾病 重新「編輯」嬰兒DNA消除病魔創科學奇蹟
美國費城兒童醫院(Children’s Hospital of Philadelphia)一名年僅15個月大的男嬰KJ(KJ Muldoon),近日成為全球第一個接受「客製化DNA基因重寫療法」成功「移除」致命遺傳疾病的嬰兒。KJ出生不久後,就被醫師診斷出罹患極為罕見且致命的CPS1缺乏症(CPS1 deficiency),這種疾病會導致其肝臟無法有效分解體內氨氣,若不立即處理,將可能在數日內導致腦部永久損傷甚至死亡。根據《太陽報》報導指出,當時醫師發現KJ血液中的氨濃度異常升高,於是便立即進行透析,以便排除KJ體內的氨。原本是計畫馬上安排KJ住院,等待KJ長大後,能夠接受肝臟移植,而這也代表著,KJ有可能童年時期都得待在醫院病房。但費城兒童醫院與賓州大學(University of Pennsylvania)一支研究團隊,嘗試採取突破性作法,研究團隊為KJ量身訂製一項專屬療法,運用CRISPR-Cas9技術,透過分子剪刀形式的酶,針對性地切除KJ體內導致疾病的突變DNA,再植入正常的序列,修正其基因錯誤。這種療法不同於傳統基因療法的通用設計,而是為KJ本人所專屬,因他體內的突變為罕見且個別的類型。領導醫療計畫的賓州大學遺傳學與基因編輯專家穆蘇努魯(Kiran Musunuru)表示,這是一種真正意義上的個人化醫療,也是對基因編輯技術潛力的首次臨床驗證。他與CHOP的兒童遺傳學家阿倫斯尼克拉斯(Rebecca Ahrens-Nicklas)合作。2025年2月,KJ開始接受第一劑低劑量藥物輸注。幾天內,KJ的身體明顯改善,能攝取更多蛋白質卻未再出現氨濃度上升,醫師也逐步減少KJ的降氨藥物,並在兩個月內進行第二與第三劑的高劑量療程,至今未出現嚴重副作用。妮可表示,KJ從原本只有四磅重的虛弱寶寶,如今已是健康、有活力的嬰兒,且原本預定的肝臟移植計畫也已暫停。報導中也提到,KJ是極少數能及時接受此類療法的個案。阿倫斯尼克拉斯回憶,當初他們最擔心的不是技術困難、不是失敗,而是擔心如此療法,可能為KJ的家庭帶來虛假的希望。而這項技術之所以能如此發展迅速,歸功於穆蘇努魯於2021年疫情後與團隊重返實驗室時,已預先投入基因療法的設計與模擬。目前,這項成果已於15日刊登於《新英格蘭醫學期刊》(New England Journal of Medicine)。美國食品藥物管理局(Food and Drug Administration,FDA)負責監督這項療法的前主管馬克斯(Peter Marks)表示,雖然每名病患需設計不同的基因修補方式,但其平台與製程具高度可複製性,極可能成為未來罕見疾病治療的標準模式。目前,KJ已逐步恢復成像一般嬰兒的體質,家人與醫師都抱持審慎樂觀態度,雖然療效仍需長期觀察,但這場對抗罕病的實驗已成功開啟了基因療法嶄新的篇章。

新冠連5周升溫!疫苗打氣增2成 單日2810人創新高紀錄
新冠疫情連5周升溫!疾管署預估高峰期將會落在5~6月之間,隨著愈來愈多民眾確診,新冠疫苗打氣也直線往上衝,根據疾管署最新統計,本周近四日(5/12-5/15)新冠疫苗接種人數共計9,092人,較上周同期(5/5-5/8)接種7,512人增加21%,昨(15)日接種2810人更創約7周來單日新高,顯示民眾接種意願提升。疾管署表示,公費新冠疫苗庫存仍有約318萬劑,供應無虞,請年齡滿6個月以上民眾踴躍接種,在疫情高峰前提升自我免疫防護,以接種疫苗降低新冠中重症發生風險。疾管署說明,世界衛生組織(WHO)昨日公布最新新冠疫苗選株會議結論,認為目前的新冠JN.1疫苗仍具足夠保護力。由於全球流行主流仍為JN.1衍生的變異株,世衛專家小組於5/6-5/7開會評估目前使用的新冠疫苗株(JN.1或KP.2),結論為目前疫苗株仍有保護效果、為可持續建議選用的合適疫苗株,也同時建議新變異株LP.8.1為合適的替代疫苗株選項。由於五月中下旬美國食品藥物管理局(FDA)、歐洲醫藥管理局(EMA)也將陸續開會決定新冠疫苗選株建議,疾管署將視上述結論是否一致,必要時提ACIP討論我國秋冬新冠疫苗選株建議。疾管署提醒,雖然新冠病毒感染多為輕症或無症狀,但病程仍有機會發展為中重症。由於國內疫情持續上升,滿6個月以上且尚未接種新冠 JN.1疫苗者別輕視疾病威脅,應儘速接種。此外,已接種1劑且間隔6個月(180天)的65歲以上長者等3類高風險對象,應再接種第2劑,以提升免疫保護力。針對民眾抱怨買不到新冠快篩,食藥署副署長王德原表示,有關家用新冠快篩試劑國內已核准4張許可證,相關業者分別為寶齡富錦生技股份有限公司、台塑生醫科技股份有限公司以及亞培快速診斷設備股份有限公司,另專業人士用新冠快篩試劑已核准6張許可證,目前整體供應量能充足。王德原說,已主動聯繫四大超商、連鎖藥局等通路,針對家用新冠快篩試劑請其協助鋪貨/備貨,以維持國內防疫量能,相關通路也表示會盡力配合政府政策,但目前仍須視各門市市場需求,不一定全省通路皆會鋪貨,建議民眾可至較大型的連鎖藥局購買。